
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 |  | 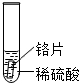 | 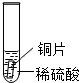 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象 |
分析 【作出猜想】:根据三种金属的活动性顺序进行猜想;
【设计与实验】根据铜的活动性顺序位于氢的后面分析现象;
【结论与解释】(1)根据实验的现象得出结论;(2)根据金属的表面常有一层金属氧化物会影响金属和溶液的反应分析;
【知识运用】根据在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来分析并写出反应的方程式.
解答 解:【作出猜想】:三种金属的活动性顺序可能存在三种情况:猜想1为Cr>Fe>Cu;猜想2为Fe>Cu>Cr,故猜想3答案:Fe>Cr>Cu;
【设计与实验】因为铜的活动性顺序位于氢的后面,因此不能和酸反应,表现为无现象;
【结论与解释】(1)试管1中实验现象铁片表面产生气泡较慢,溶液变为浅绿色,可知金属铁在金属活动顺序中排在氢前,根据铬片表面产生气泡较快,溶液变为蓝色,从而得出铬也排在氢前且铬比铁活泼,因为铜不能和稀硫酸反应生成氢气,可知铜排在氢的后面,故猜想1.Cr>Fe>Cu正确;
(2)因为金属的表面常有一层金属氧化物会影响金属和溶液的反应,因此实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应;
【知识运用】因为“铬片表面产生气泡较快溶液变为蓝色”,可知金属铬比铁活泼强,故铬能和硫酸铜反应生成硫酸铬和铜,则反应的化学方程式为:Cr+CuSO4=Cu+CrSO4;
答案:
【作出猜想】:3.Fe>Cr>Cu;
【设计与实验】无明显现象
【结论与解释】(1)I; (2)除去金属表面的氧化膜.
【知识运用】铬片表面有红色固体生成; Cr+CuSO4=Cu+CrSO4.
点评 本题是对金属活动性顺序的考查,运用实验探究金属的活动性顺序,考查了实验探究的过程,注重学生运用实验分析实验能力的培养.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
 元素周期表是学习和研究化学的重要工具.根据如图提供的信息,下列判断不正确的是( )
元素周期表是学习和研究化学的重要工具.根据如图提供的信息,下列判断不正确的是( )| A. | 元素所在的周期数等于其原子的电子层数 | |
| B. | 镁离子核外有两个电子层,其离子符号是Mg+2 | |
| C. | 第二、三周期元素的原子从左至右最外层电子数逐渐增多 | |
| D. | 钾元素的原子结构示意图为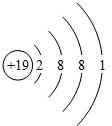 ,与钠元素的化学性质相似 ,与钠元素的化学性质相似 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 现象 | 结论 |
| 该废液中一定没有盐酸 | ||
| 该废液中一定含有Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaCl2、KNO3、NaCl | B. | NaOH、CuCl2、HCl | ||
| C. | AgNO3、KNO3、HCl | D. | H2SO4、NaCl、Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 “太阳能光伏发电系统”在交通、通讯、海洋、气象、光伏电站、太阳能建筑等领域中,具有不同程度的应用.白天在光照条件下,太阳能电池组件产生已经的电动势,形成太阳能电池方阵,再对蓄电池进行充电,将电能储存起来,晚上,将直流电转换成交流电,输送到配电柜进行供电.请回答下列各题:
“太阳能光伏发电系统”在交通、通讯、海洋、气象、光伏电站、太阳能建筑等领域中,具有不同程度的应用.白天在光照条件下,太阳能电池组件产生已经的电动势,形成太阳能电池方阵,再对蓄电池进行充电,将电能储存起来,晚上,将直流电转换成交流电,输送到配电柜进行供电.请回答下列各题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 化学是研究物质的组成、结构、性质及变化规律的科学.
化学是研究物质的组成、结构、性质及变化规律的科学.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com