【答案】
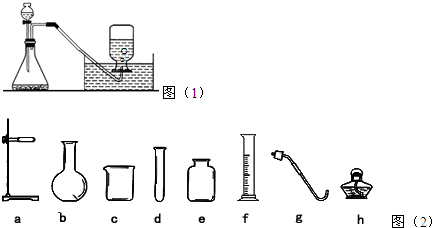
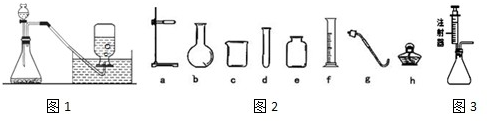
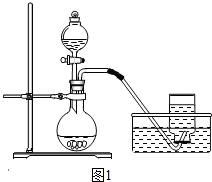
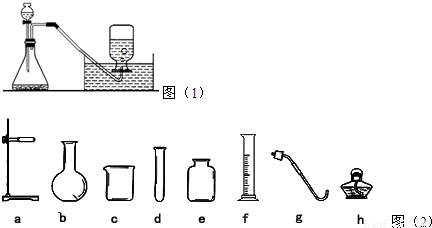
分析:(1)该装置可用于固体与液体不加热制取气体的反应;制取气体的装置实验前一定要检查装置的气密性.
(2)凡是固体与液体常温下制取气体、能用排水法收集的气体都可用此装置.
(3)根据锥形瓶所起的作用进行分析解答.
(4)根据题意可知组装成氧气发生装置有酒精灯,即为“固体加热型”装置,反应原理为加热高锰酸钾或加热氯酸钾的方法.
(5)根据题意:在加热或加入二氧化锰后能复燃,进行分析解答.
解答:解:(1)该装置用于固体与液体不加热制取气体的反应,所以用该装置制取氧气应选用双氧水和二氧化锰来制取,化学方程式是:2H
2O
2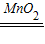
2H
2O+O
2↑;制取气体的装置实验前一定要检查装置的气密性;氧气密度比空气大,可用向上排空气法收集.
(2)凡是固体与液体常温下制气体的反应都可用此装置,实验室制二氧化碳用的药品是大理石和稀盐酸,制氢气用的药品是锌粒和稀硫酸,都是常温下反应,但二氧化碳能溶于水,不能用排水法收集,故此装置还可用于制取氢气.
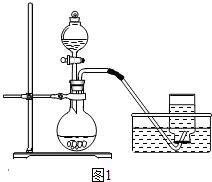
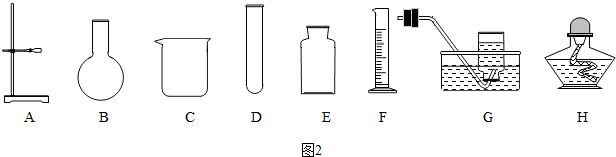
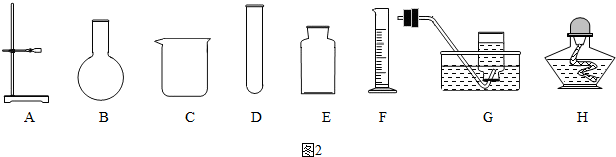
(3)此装置中的锥形瓶可用上图中的烧瓶、试管、集气瓶等代替.
(4)用图(2)中的a、d、g、h仪器组装成氧气发生装置中有酒精灯,即为“固体加热型”装置,反应原理为加热高锰酸钾或加热氯酸钾的方法.
(5)带火星的木条在盛过氧化氢溶液的试管中不能复燃,而在加热或加入二氧化锰后能复燃,可以看出温度、催化剂影响了过氧化氢分解速率.带火星的木条在空气中不能复燃,而在纯氧气中能复燃,氧气的体积分数(或浓度)与带火星的木条能否复燃有关.
故答案为:
(1)2H
2O
2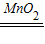
2H
2O+O
2↑;检查装置的气密性;向上排空气法.
(2)氢气.
(3)b、d、e.
(4)高锰酸钾.
(5)温度、催化剂;氧气的体积分数(或浓度).
点评:本题综合性较强,考查学生对实验室制取氧气的反应原理的理解与应用及灵活运用进行分析问题、解决问题的能力.

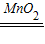 2H2O+O2↑;制取气体的装置实验前一定要检查装置的气密性;氧气密度比空气大,可用向上排空气法收集.
2H2O+O2↑;制取气体的装置实验前一定要检查装置的气密性;氧气密度比空气大,可用向上排空气法收集.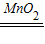 2H2O+O2↑;检查装置的气密性;向上排空气法.
2H2O+O2↑;检查装置的气密性;向上排空气法.

 一线名师提优试卷系列答案
一线名师提优试卷系列答案