
【题目】水和溶液在生命活动和生产生活中起着十分重要的作用。
(1)保持水的化学性质的最小微粒是________。
(2)“生命吸管”是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等。其中活性炭起到________的作用。
(3)如下图,用一块棉手帕,在盛有乙醇的体积分数为70%的酒精溶液的烧杯中浸泡,待均匀湿透后取出。将浸透的手帕舒展开,用镊子夹住两角,在火焰上点燃,让它燃烧。当火焰熄灭后,手帕完好无损。从燃烧的条件看,手帕完好无损的原因是________。

(4)附在衣服上的碘渍,用酒精可以洗掉,但用水不易直接洗掉,其原因是________。
(5)根据如下图中A、B两种物质的溶解度曲线,回答下列问题.

①把t℃时150gA物质的饱和溶液稀释成20%,需加水________g。
②若A固体中含有少量的B,可用________方法提纯A。
【答案】 水分子 吸附 温度没有达到手帕的着火点 碘易溶于酒精,不易溶于水 100 冷却热饱和溶液(或降温结晶)
【解析】(1)保持水的化学性质的最小微粒是水分子,分子是保持物质化学性质的最小微粒。(2)活性炭起到吸附的作用,活性炭具有吸附性,可以吸附色素和异味。(3)将用70%的酒精溶液浸透的手帕舒展开,用镊子夹住两角,在火焰上点燃,让它燃烧。当火焰熄灭后,手帕完好无损。从燃烧的条件看,手帕完好无损的原因是温度没有达到手帕的着火点,酒精着火点比较低,手帕着火点比较高。(4)附在衣服上的碘渍,用酒精可以洗掉,但用水不易直接洗掉,其原因是碘易溶于酒精,不易溶于水,根据相似相容原理。(5)根据所学知识和题中信息知,①t℃时,A溶解度是50g,设将150gA物质的饱和溶液稀释成20%,需加水x∶根据溶液稀释前后溶质质量不变,150g×![]() ×100%=﹙150g+x﹚×20%,x=100g。 ②若A固体中含有少量的B,可用冷却热饱和溶液(或降温结晶)方法提纯A,A物质溶解度受温度影响变化较大,B物质溶解度受温度影响变化不大。
×100%=﹙150g+x﹚×20%,x=100g。 ②若A固体中含有少量的B,可用冷却热饱和溶液(或降温结晶)方法提纯A,A物质溶解度受温度影响变化较大,B物质溶解度受温度影响变化不大。
点睛∶溶解度曲线的意义①表示同一种物质在不同温度时的溶解度或溶解度随温度变化的情况;②表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小。若两种物质的溶解度曲线相交,则在该温度下两种物质的溶解度相等;③根据溶解度曲线可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法;④根据溶解度曲线能进行有关的计算。


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:
【题目】某研究性学习小组设计了测定纯碱(Na2CO3)样品(假设只含NaCl杂质)中Na2CO3质量分数的实验方案,请你参与他们的探究活动,请回答下列问题:(不考虑原装置内空气的影响)A组同学设计了如图1的实验装置。
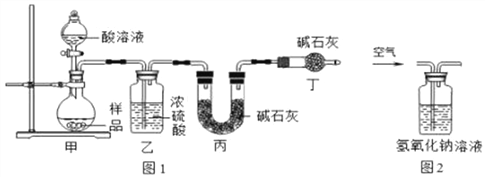
(1)实验时,在装药品前需组装好如图仪器,并___________。
(2)装置乙的作用是____________;
(3)装置丁的作用是____________。(填字母)
A.吸收Na2CO3与酸溶液反应产生CO2 B.防止空气中二氧化碳和水蒸气进入装置丙中 C.干燥二氧化碳
(4)实验中如果滴加酸溶液的速度过快,会导致测得样品中碳酸钠的质量分数_____(填“偏大”或“偏小”或“无影响”)。
(5)B组同学认为A组同学的方案存在问题,即使操作规范,测定结果也会偏低,理由是_____,应该将装置甲中双孔橡胶塞换成三孔橡胶塞,并在甲的左边连接上图2装置,实验结束后缓缓通入一段时间空气,目的是_____,其中NaOH溶液的作用是_____.若没有图2装置,直接通入空气,则会导致测得结果_____(填“偏大”或“偏小”或“无影响”)。
(6)你认为实验时加入的酸溶液最好是_____(填“稀盐酸”或“稀硫酸”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】M、N两种物质的溶解度曲线如图所示。t2℃时,分别将50 g的M、N固体加入到100 g水中,搅拌。下列说法不正确的是( )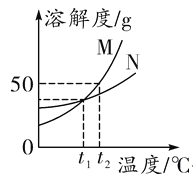
A. t2 ℃时,N固体不能完全溶解
B. t2 ℃时,M的饱和溶液中溶质的质量分数为50%
C. M的溶解度受温度变化的影响大于N
D. 分别将上述t2 ℃时 M、N的溶液降温到t1 ℃,得到M、N溶液的质量一定相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁是一种白色的粉末,其外观、物理性质与氧化镁相似。过氧化镁在常温下比较稳定,但是加热时会分解生成氧气和氧化镁。写出该反应的化学方程式____________。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2 。同时温度升高,说明该反应_____热量(填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁【Mg2( OH)2CO3】和30%的过氧化氢溶液来制取过氧化镁。
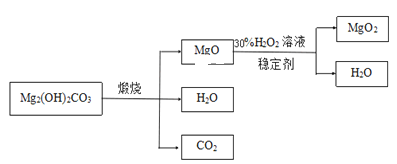
【资料】①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳;
②氧化镁与过氧化氢反应放出大量的热。
(3)检测煅烧过程碱式碳酸镁已完全分解的方法是_________________(写出具体的操作和现象);上述生产过程加入稳定剂的作用是__________________。
(4)用上述碱式碳酸镁在 550、600、650 及 700 ℃ 下煅烧一定的时间生成氧化镁,再用上述条件制备的氧化镁分别与 30% 双氧水反应生成过氧化镁的产率如下面的图1和图2。碱式碳酸镁煅烧的温度适宜控制在_______℃,煅烧的时间适宜控制在______h。
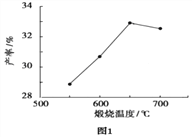
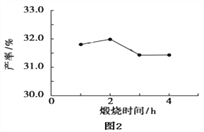
三.过氧化镁的纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。
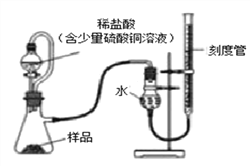
①装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管读数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管读数为122mL。
(5)实验步骤中,装入药品前应先(_________)。
(6)稀盐酸中放入少量硫酸铜溶液的目的是______________。
(7)根据上面实验数据计算样品中过氧化镁的质量分数(写出具体的计算过程,该实验条件下O2密度为1.429g/L)。 ____________
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是(_______)
A.生成的氧气有少量溶于水 B.未等装置冷却到室温就开始读数
C.杂质与盐酸反应能产生少量的气体 D.滴入的稀盐酸占了一部分气体的体积
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活密切相关。请回答以下问题:
① 活性炭可去除冰箱中异味,利用活性炭的______性。
② 土壤里撒入适量的石灰,使土壤的______(填“酸性”或“碱性”)减弱。
③ 金属冶炼可使矿石中金属元素转变为______(填“化合”或“游离”)态。 写出氢气还原氧化铜的化学方程式________。
④ 自来水生产中通入氯气的作用是______;实验室制取氯气的化学方程式是
4HCl(浓) + MnO2![]() X + Cl2↑+ 2H2O ,则 X 的化学式为______。
X + Cl2↑+ 2H2O ,则 X 的化学式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色固体,可能是碳酸钠、氯化钠、氢氧化钠、硝酸钡中的一种或几种,为确定 成分,进行如下实验(硝酸钠溶液和硝酸钡溶液均呈中性):
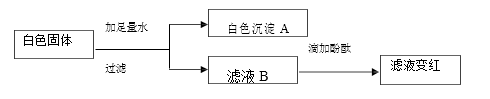
① 白色沉淀 A 是______,化学方程式是______。
② 滤液 B 中溶质一定有______,可能有______(任写一种情况); 为确定白色固体中可能存在的物质,进一步对滤液 B 进行实验,步骤如下:
Ⅰ. 重新取滤液 B,滴加过量的试剂 X; Ⅱ. 向Ⅰ中的溶液滴加过量的稀硝酸; Ⅲ. 向Ⅱ中的溶液滴加试剂 Y。完成填空:试剂 X 是__溶液(填“氯化钡”或“硝酸钡”);试剂 Y 是_________溶液。 若_______ (写现象及对应的步骤编号),能确定白色固体中含有氢氧化钠。 若_______(写现象及对应的步骤编号),能确定白色固体中含有氯化钠。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列问题的研究中,未利用对比实验思想方法的是( )
A. 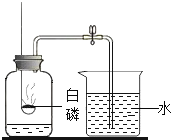 研究空气中氧气含量
研究空气中氧气含量
B. 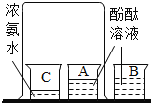 研究分子的运动
研究分子的运动
C. 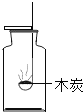 研究木炭在氧气中燃烧
研究木炭在氧气中燃烧
D.  研究二氧化碳与水的反应
研究二氧化碳与水的反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】微量元素是人体必需的,摄入不足不利于人体健康,硒被誉为“抗癌元素”。根据如图提供的硒的有关信息,下列说法中,正确的是 ( )

A. 硒属于金属元素 B. 硒原子中的核内质子数是34
C. 硒的原子结构示意图中x=4 D. 硒的相对原子质量是78.96 g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小红家喜欢养金鱼,但金鱼存活的时间总是不长,她上网查阅资料得知:鱼缸中每升水的溶氧量低于0.003g时,鱼就会死亡。过氧化钙(CaO2)是一种化学增氧剂,其反应原理是2CaO2+2H2O==2Ca(OH) 2+O2↑请回答:
(1)氧气在水中的溶解度随温度的升高而_____。
(2)小红将2.88g过氧化钙放入盛有200L水的鱼缸中,请你通过计算分析,当过氧化钙完全反应后,鱼缸中水的溶氧量是否符合最低要求?(假设产生的氧气完全溶入水,其他因素忽略不计)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com