
分析 根据方程式的写法考虑;根据反应物中和生成物中都有的物质考虑;根据碳酸氢钠受热易分解分析.
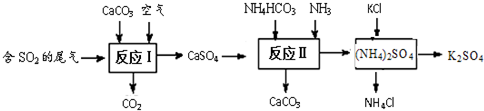
解答 解:①反应物是CaSO4、NH4HCO3、NH3生成物是CaCO3和(NH4)2SO4,碳酸钙后面标上沉淀符号.
②由图示可知反应物有二氧化硫、碳酸钙、空气;反应过程中生成物有:二氧化碳、硫酸钙、碳酸钙、氯化铵、硫酸钾,所以在反应物中和生成物中都有的物质是碳酸钙,所以流程中可循环使用的物质是碳酸钙;
③碳酸氢钠受热易分解,为防止NH4HCO3受热分解,所以反应Ⅱ的温度需控制在60~70℃.
④副产物可做氮肥或化肥等.
故答案为:①CaSO4+NH4HCO3+NH3═CaCO3↓+(NH4)2SO4;
②CaCO3;
③防止NH4HCO3受热分解;
④氮肥或化肥等.
点评 本题难度不大,可依据已有的知识解答.


科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解,分液漏斗可以通过调节活塞控制液体的滴加速度,请根据如图回答以下问题:
过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解,分液漏斗可以通过调节活塞控制液体的滴加速度,请根据如图回答以下问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 | |
| B. | 二氧化碳+水--→碳酸 | |
| C. | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 | |
| D. | 碱式碳酸铜$\stackrel{加热}{→}$氧化铜+水+二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 有关反应的化学方程式 |
| 方案一 | (1)Fe+H2SO4=FeSO4+H2↑ (2)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O |
| 方案二 | (1)CuO+H2SO4=CuSO4+H2O (2)Fe+CuSO4=Cu+FeSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
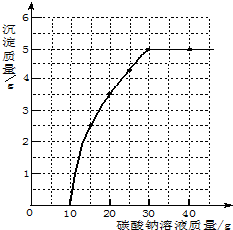 实验室用过量的稀盐酸和大理石制取CO2,取100g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.
实验室用过量的稀盐酸和大理石制取CO2,取100g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
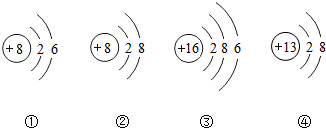
| A. | ④表示的是阳离子 | |
| B. | ?①③属于同种元素,?②④属于另一种元素 | |
| C. | ?②④形成的化合物是Al2O3 | |
| D. | ①③的化学性质相似 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com