
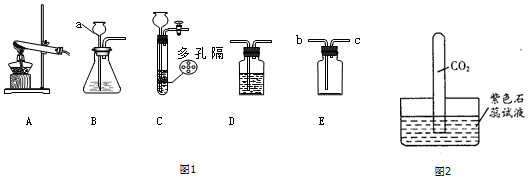
分析 长颈漏斗方便加液体药品,在加入药品前,应首先检查装置的气密性;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳可以用浓硫酸干燥.图2中,试管中产生的现象是:试管中液面上升,紫色变红色;是因为二氧化碳和水反应生成碳酸;若将图2装置中的紫色石蕊溶液换成澄清石灰水,现象是试管中液面上升,澄清石灰水变浑浊;是因为二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)如果用高锰酸钾或氯酸钾制氧气就需要加热,在加入药品前,应首先检查装置的气密性;故答案为:A;检查装置的气密性;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加.;二氧化碳可以用浓硫酸干燥;如果用E装置收集该气体,则气体从长管进入,因为二氧化碳的密度比空气的密度大;故答案为:稀盐酸;CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸;b;
(4)C装置的优点是:可以控制反应的发生和停止;故答案为:可以控制反应的发生和停止;
(5)图2中,试管中产生的现象是:试管中液面上升,紫色变红色;是因为二氧化碳和水反应生成碳酸;故答案为:①试管中液面上升,紫色变红色;②CO2+H2O=H2CO3;
(6)若将图2装置中的紫色石蕊溶液换成澄清石灰水,现象是试管中液面上升,澄清石灰水变浑浊;是因为二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水;故答案为:①试管中液面上升,澄清石灰水变浑浊;②CO2+Ca(OH)2=CaCO3↓+H2O;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥和性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 28% | B. | 32% | C. | 40% | D. | 50% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 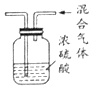 除去氧气中的水蒸气 | B. | 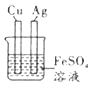 验证Fe、Cu、Ag的金属活动性强弱 | ||
| C. | 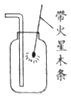 检验O2是否收集满 | D. | 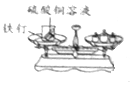 验证质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 导体:石墨、铜丝、食盐水溶液 | B. | 盐类:烧碱、纯碱、小苏打 | ||
| C. | 混合物:合金、冰水共存物、碘酒 | D. | 非晶体:石蜡、海波、玻璃 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 切菜的刀钝了要磨一磨-为了减小压强 | |
| B. | 铝制品耐腐蚀-铝的化学性质稳定 | |
| C. | 揭开正在煮东西的锅盖时,会看到“白气”-气体的液化 | |
| D. | 煮粥时纯碱放多了加醋调节-发生了中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
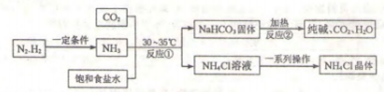
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - | |
| NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.5 | 77.3 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com