
| A. | 加入生石灰 | B. | 升高温度 | C. | 降低温度 | D. | 加入水 |
分析 氢氧化钙的溶解度随温度升高而减小,多数物质的不饱和溶液变为饱和溶液,常用的方法有:增加溶质、蒸发溶剂、降低温度,据此进行分析判断.
解答 解:A、加入生石灰,生石灰能与水反应生成氢氧化钙,能使接近饱和的Ca(OH)2溶液变成饱和溶液,故选项措施正确.
B、氢氧化钙的溶解度随温度升高而减小,升高温度,氢氧化钙的溶解度减小,能使接近饱和的Ca(OH)2溶液变成饱和溶液,故选项措施正确.
C、氢氧化钙的溶解度随温度升高而减小,降低温度,氢氧化钙的溶解度增大,接近饱和的Ca(OH)2溶液仍为不饱和溶液,故选项措施错误.
D、加入水,接近饱和的Ca(OH)2溶液能继续溶解溶质,溶液仍为不饱和溶液,故选项措施错误.
故选:AB.
点评 本题难度不大,增加溶质、蒸发溶剂都可以把不饱和溶液变成饱和溶液,但改变温度使不饱和溶液变成饱和溶液时要具体分析溶解度与温度的关系.


科目:初中化学 来源: 题型:解答题
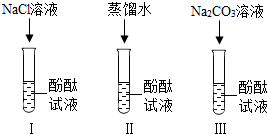 小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请小宁、小明和你一起探究并完成下列问题:
小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请小宁、小明和你一起探究并完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | pH=0的溶液 | B. | pH=5的溶液 | C. | pH=7的溶液 | D. | pH=11的溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaHCO3 H2SO4 HCl | B. | KCl CuCl2 NaOH | ||
| C. | BaCl2 H2SO4 AgNO3 | D. | FeCl3 KCl NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 点燃纸张,在火焰上方罩上光洁干燥的冷玻璃杯 | 玻璃杯内壁有水雾 | 纸张燃烧的产物有水. |
| 把玻璃杯迅速倒转过来倒入澄清石灰水 | 石灰水变浑浊 | 纸张燃烧的产物有二氧化碳. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
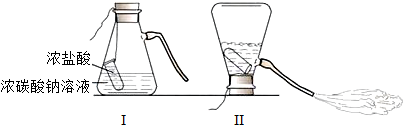 某化学兴趣小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究.
某化学兴趣小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com