
”¾ĢāÄæ”æĪŖĢ½¾æĢ¼»¹ŌŃõ»ÆĶµÄ×ī¼ŃŹµŃéĢõ¼ž£¬ÓĆľĢæ·ŪŗĶŃõ»ÆĶµÄøÉŌļ»ģŗĻĪļ1”«2.5g½ųŠŠĻµĮŠŹµŃ锣
£Ø²éŌÄ׏ĮĻ£©Ģ¼»¹ŌŃõ»ÆĶµĆµ½µÄĶÖŠæÉÄÜŗ¬ÓŠÉŁĮæŗģÉ«µÄŃõ»ÆŃĒĶ£ØĘäÖŠĶŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+1¼Ū£©”£
£Ø½ųŠŠŹµŃ飩ŹµŃé1£ŗȔ֏Įæ±ČĪŖ1£ŗ11µÄľĢæ·ŪŗĶŃõ»ÆĶ»ģŗĻĪļ1.3g£¬½ųŠŠŹµŃ锣
ŠņŗÅ | 1©1 | 1©2 |
×°ÖĆ |
|
|
·“Ó¦ŗóĪļÖŹµÄŃÕÉ«”¢×“Ģ¬ | ŗŚÉ«·ŪÄ©ÖŠ»ģÓŠÉŁĮæŗģÉ«¹ĢĢå | ŗģÉ«¹ĢĢåÓŠ½šŹō¹āŌ󣬻ģÓŠ¼«ÉŁĮæŗŚÉ«ĪļÖŹ |
ŹµŃé2£ŗČ”Ņ»¶ØĮæµÄ»ģŗĻĪļ£¬ÓĆ1©2×°ÖĆ½ųŠŠŹµŃ锣
ŠņŗÅ | ľĢæ·ŪÓėŃõ»ÆĶµÄÖŹĮæ±Č | ·“Ó¦ŗóĪļÖŹµÄŃÕÉ«”¢×“Ģ¬ | |
2©1 | 1£ŗ9 | ŗģÉ«¹ĢĢåÓŠ½šŹō¹āŌó | »ģÓŠÉŁĮæŗŚÉ«ĪļÖŹ |
2©2 | 1£ŗ10 | »ģÓŠŗÜÉŁĮæŗŚÉ«ĪļÖŹ | |
2©3 | 1£ŗ11 | »ģÓŠ¼«ÉŁĮæŗŚÉ«ĪļÖŹ | |
2©4 | 1£ŗ12 | ĪŽŗŚÉ«ĪļÖŹ | |
2©5 | 1£ŗ13 | »ģÓŠ½Ļ¶ąŗŚÉ«ĪļÖŹ | |
£Ø1£©Ńõ»ÆŃĒĶµÄ»ÆѧŹ½ĪŖ_____”£
£Ø2£©ŹµŃé1©2ÖŠ£¬Ö¤Ć÷²śÉśĮĖ¶žŃõ»ÆĢ¼µÄĻÖĻóŹĒ_____£¬Ļą¹ŲµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ_____”£
£Ø3£©ŹµŃé1©2ÖŠ£¬“ż·“Ó¦½įŹų£¬ĻČ½«µ¼Ęų¹Ü“ÓŹÆ»ŅĖ®ÖŠČ”³ö£¬Č»ŗó¹Ų±ÕÖ¹Ė®¼Š£¬ČĆ²śĪļ×ŌČ»ĄäČ“”£Čō²»¹Ų±ÕÖ¹Ė®¼Š£¬æÉÄܳöĻÖµÄĪŹĢāŹĒ_____”£
£Ø4£©ŹµŃé1µÄÄæµÄŹĒ_____”£
£Ø5£©ŹµŃé2µÄ½įĀŪŹĒ_____”£
£Ø·“Ė¼ÓėĘĄ¼Ū£©
£Ø1£©ÓŠĶ¬Ń§½ØŅéÓĆ³¬ĻøĢæ·ŪÓėŃõ»ÆĶ·ŪÄ©½ųŠŠŹµŃ锣ÄćČĻĪŖÕāŃł½ØŅéµÄĄķÓÉŹĒ_____”£
£Ø2£©ŹµŃé2Ī“½ųŠŠÖŹĮæ±ČĪŖ1£ŗ14µÄŹµŃ飬ĄķÓÉŹĒ_____”£
”¾“š°ø”æCu2O ³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē CO2+Ca£ØOH£©2£½CaCO3”ż+H2O æÕĘų»į½ųČėŹŌ¹ÜÖŠ£¬Ź¹Éś³ÉµÄ×ĘČȵÄĶÖŲŠĀ±»Ńõ»Æ Ģ½¾æŃõ»ÆĶÓėľĢæµÄŹÜČČĆ껿¶ŌĘä·“Ó¦µÄÓ°Ļģ ľĢæÓėŃõ»ÆĶÖŹĮæ±ČĪŖ1£ŗ12Ź±Ē”ŗĆĶźČ«·“Ó¦£¬Ņņ“ĖľĢæÓėŃõ»ÆĶ·“Ó¦µÄ×ī¼ŃÖŹĮæ±ČĪŖ1£ŗ12 Ōö“óĮĖ·“Ó¦ĪļÖ®¼äµÄ½Ó“„Ć껿£¬·“Ó¦½ųŠŠµĆøü³ä·Ö ľĢæÓėŃõ»ÆĶµÄÖŹĮæ±ČĪŖ1£ŗ13Ź±£¬Ńõ»ÆĶŅŃ¹żĮæ”””£
”¾½āĪö”æ
[½ųŠŠŹµŃé]£Ø1£©Ńõ»ÆŃĒĶÖŠ£¬ĶŌŖĖŲĻŌ+1¼Ū£¬ŃõŌŖĖŲĻŌ-2¼Ū£¬ĖłŅŌŃõ»ÆŃĒĶµÄ»ÆѧŹ½ĪŖCu2O£»
£Ø2£©¶žŃõ»ÆĢ¼ÓėĒāŃõ»ÆøĘ·“Ӧɜ³ÉĢ¼ĖįøĘ°×É«³ĮµķŗĶĖ®£¬»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗCO2+Ca£ØOH£©2=CaCO3”ż+H2O£»ĖłŅŌ¶žŃõ»ÆĢ¼ÄÜŹ¹³ĪĒåµÄŹÆ»ŅĖ®±ä»ė×Ē£¬¹ŹÖ¤Ć÷Éś³ÉĮĖCO2µÄĻÖĻóŹĒ³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£»
£Ø3£©“ż·“Ó¦½įŹų£¬ĻČ½«µ¼Ęų¹Ü“ÓŹÆ»ŅĖ®ÖŠČ”³ö£¬Č»ŗó¹Ų±ÕÖ¹Ė®¼Š£¬ČĆ²śĪļ×ŌČ»ĄäČ“£»Čō²»¹Ų±ÕÖ¹Ė®¼Š£¬æÉÄܳöĻÖµÄĪŹĢāŹĒæÕĘų»į½ųČėŹŌ¹ÜÖŠ£¬Ź¹Éś³ÉµÄ×ĘČȵÄĶÖŲŠĀ±»Ńõ»Æ£»
£Ø4£©ŹµŃé1ÖŠŹµŃé1-1»ģŗĻĪļµÄŹÜČČĆ껿“óÓŚŹµŃé1-2ÖŠ»ģŗĻĪļµÄŹÜČČĆ껿£¬¹ŹŹĒĢ½¾æŃõ»ÆĶÓėľĢæµÄŹÜČČĆ껿¶ŌĘä·“Ó¦µÄÓ°Ļģ£»
£Ø5£©ŹµŃé2Ģį¹©µÄŹż¾ŻŅŌ¼°ŹµŃéĻÖĻóæÉŅŌ擳ö£¬Ä¾ĢæÓėŃõ»ÆĶÖŹĮæ±ČĪŖ1£ŗ12Ź±Ē”ŗĆĶźČ«·“Ó¦£¬Ņņ“ĖľĢæÓėŃõ»ÆĶ·“Ó¦µÄ×ī¼ŃÖŹĮæ±ČĪŖ1£ŗ12£»
[·“Ė¼ÓėĘĄ¼Ū]£Ø1£©³¬ĻøĢæ·ŪÓėŃõ»ÆĶ·ŪÄ©µÄ½Ó“„Ć껿“󣬷“Ó¦øü³ä·Ö£»
£Ø2£©Ä¾ĢæÓėŃõ»ÆĶµÄÖŹĮæ±ČĪŖ1£ŗ13Ź±£¬Ńõ»ÆĶŅŃ¹żĮ棬ĖłŅŌƻӊ±ŲŅŖ½ųŠŠÖŹĮæ±ČĪŖ1£ŗ14µÄŹµŃ锣



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ®ŹĒČĖĄąÉē»į·¢Õ¹µÄÖŲŅŖ׏Ō“”£
(1)ŌŚĢģČ»Ė®ÖŠ¼ÓČėĆ÷·ÆµÄ×÷ÓĆŹĒ_________________________”£
(2)ÓĆ_______æÉĒų±šÓ²Ė®ŗĶČķĖ®,Éś»īÖŠ³£ÓĆ_________µÄ·½·Ø½µµĶĖ®µÄÓ²¶Č”£
(3)Ė®µē½āµÄ»Æѧ·½³ĢŹ½ĪŖ____________,Õż¼«ŗĶøŗ¼«²śÉśĘųĢåµÄĢå»ż±ČĪŖ___________.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§ĄūÓĆŅŌĻĀÓĆĘ·½ųŠŠ¶žŃõ»ÆĢ¼ŠŌÖŹŹµŃ锣

£ØŹµŃé1£©ĻņĶ¼1¼ÆĀśCO2µÄČķĖÜĮĻĘæÖŠ£¬ŃøĖŁµ¹Čė°ėĘæÕōĮóĖ®£¬Šż½ōĘæøĒ”£³ä·ÖÕńµ“£¬¹Ū²ģµ½ĖÜĮĻĘæ±ä±ń£¬ŌŅņŹĒ________”£
£ØŹµŃé2£©ŌŚĶ¼2µćµĪ°å¢Ł¢ŚĮ½øöæ×ÄŚø÷µĪ¼Ó2µĪ×ĻÉ«ŹÆČļČÜŅŗ£»ŌŁĻņ¢Łæ×ÖŠµĪ¼Ó5µĪŹµŃé1ĖÜĮĻĘæÖŠµÄŅŗĢ壬Ļņ¢Śæ×ÖŠµĪ¼Ó5µĪÕōĮóĖ®£¬¹Ū²ģµ½¢Łæ×ÖŠ×ĻÉ«ŹÆČļ±äŗģ£¬±äŗģµÄŌŅņŹĒ_____(ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾)”£¢Śæ×ÖŠµĪ¼ÓµČĮæÕōĮóĖ®µÄÄæµÄŹĒ______”£
£ØŹµŃé3£©
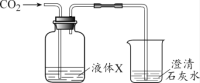
(1)ČōXĪŖ³ĪĒåŹÆ»ŅĖ®£¬¹Ū²ģµ½µÄĻÖĻóŹĒ____”£³ĪĒåŹÆ»ŅĖ®ÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____”£
(2)ČōXĪŖĒāŃõ»ÆÄĘČÜŅŗ£¬¹Ū²ģµ½³ĪĒåŹÆ»ŅĖ®ÖŠĪŽĆ÷ĻŌĻÖĻó£¬ĘäŌŅņæÉÄÜŹĒ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆČēĶ¼ŅĒĘ÷æÉĶź³É¶ąøöŹµŃ锣
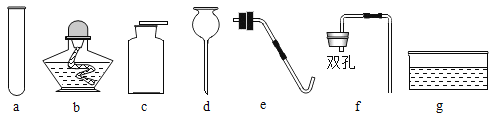
(1)ÖĘČ”ĘųĢå£ŗŹµŃéŹŅÖĘČ”¶žŃõ»ÆĢ¼µÄ»Æѧ·½³ĢŹ½ŹĒ____”£ĒėÄćĖµĆ÷ŹÕ¼Æ¶žŃõ»ÆĢ¼²»Ń”ÓĆŅĒĘ÷gµÄĄķÓÉŹĒ____”£
(2)¼ģŃéĘųĢå£ŗaÖŠŹ¢ÓŠŹŹĮæ³ĪĒåŹÆ»ŅĖ®æÉÓĆÓŚ¼ģŃ鶞Ńõ»ÆĢ¼£¬ĘäŌĄķŹĒ____(ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾)”£
(3)ÖŖŹ¶ŃÓÉģ£ŗ¼ÓČČ¹ĢĢåĢ¼ĖįĒāÄĘÖĘČ”CO2·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£ŗ2NaHCO3![]() Na2CO3+H2O+CO2”üÓ¦øĆŃ”ÓĆ·¢Éś×°ÖƵÄŅĒĘ÷³żĢś¼ÜĢØÖ®Ķā£¬»¹ŠčŅŖa”¢eŗĶ____(ĢīŅĒĘ÷Ćū³Ę)”£
Na2CO3+H2O+CO2”üÓ¦øĆŃ”ÓĆ·¢Éś×°ÖƵÄŅĒĘ÷³żĢś¼ÜĢØÖ®Ķā£¬»¹ŠčŅŖa”¢eŗĶ____(ĢīŅĒĘ÷Ćū³Ę)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČÜŅŗÓėČĖĆĒµÄÉś»īĆÜĒŠĻą¹Ų”£
£Ø1£©½«ÉŁĮæĻĀĮŠĪļÖŹ·Ö±š·ÅČėĖ®ÖŠ£¬³ä·Ö½Į°čŗóÄܵƵ½ĪŽÉ«ČÜŅŗµÄŹĒ_____£ØĢī×ÖÄø£©”£
A£®øßĆĢĖį¼Ų
B£®ĘūÓĶ
C£®°×ĢĒ
D£®Ćę·Ū
£Ø2£©ŌŚŹ¢ÓŠĖ®µÄÉÕ±ÖŠ¼ÓČėŅŌĻĀijÖÖĪļÖŹ£¬ŠĪ³ÉČÜŅŗ¹ż³ĢÖŠ£¬ĪĀ¶ČĆ÷ĻŌÉżøߵďĒ_____£ØĢī×ÖÄø£©”£
A£®ÉÕ¼ī
B£®ĻõĖįļ§
C£®ĀČ»ÆÄĘ
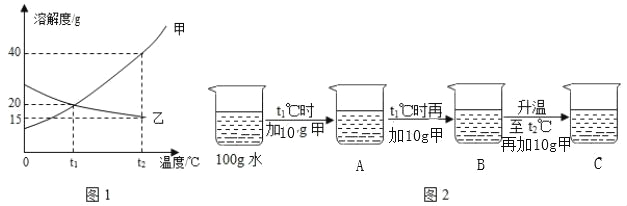
£Ø3£©ČēĶ¼1ĪŖ¼×”¢ŅŅĮ½ÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻß”£
¢ŁČܽā¶ČĖęĪĀ¶ČÉżø߶ų¼õŠ”µÄĪļÖŹŹĒ_____£ØĢī”°¼×”±»ņ”°ŅŅ”±£©”£
¢Ś°“Ķ¼2ĖłŹ¾½ųŠŠŹµŃ飬µĆµ½ĻąÓ¦ĪĀ¶ČĻĀµÄA”¢B”¢CČÜŅŗ£¬ŌŚA”¢B”¢CČżÖÖČÜŅŗÖŠŹōÓŚ±„ŗĶČÜŅŗµÄŹĒ_____£ØĢī×ÖÄø£©”£ĻņČÜŅŗCÖŠŌŁ¼ÓČė25g¼×£¬³ä·Ö½Į°č£¬»Öø“µ½t2”ꏱ£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ_____£Ø½į¹ū¾«Č·µ½0.1%£©”£
¢Ū½«t2”ꏱµÄ¼×”¢ŅŅĮ½ÖÖĪļÖŹµÄ±„ŗĶČÜŅŗ½µĪĀÖĮt1”ę£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż£ŗ¼×_____ŅŅ£ØĢī”°£¼”±”°£½”±»ņ”°£¾”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĪ¢Į£µÄ¹Ūµć»Ų“šĪŹĢā”£
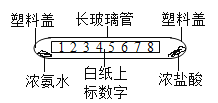
£Ø1£©ČēĶ¼ĖłŹ¾£¬½«Ź¢ÓŠÅØ°±Ė®µÄĖÜĮĻøĒĢ××”³¤²£Į§¹ÜĻĀ¶Ėŗ󣬰×Ö½Öš½„±äŗģ”£ŌŚŹŅĪĀĻĀŗģÉ«“ÓŹż×Ö1µ½“ļ8µÄĪ»ÖĆ£¬Šč2 min£»Čō½«ĖÜĮĻøĒ½žČėČČĖ®ÖŠ£¬Šč1 min”£ŗóÕߏ±¼äøü¶ĢµÄŌŅņŹĒ___________”£

£Ø2£©ŅŃÖŖ£ŗ°±Ęų(NH3)ŗĶĀČ»ÆĒā·“Ӧɜ³ÉĀČ»Æļ§£¬²śÉś°×ŃĢ”£Š“³ö»Æѧ·½³ĢŹ½£ŗ _____________”£ČēĶ¼ĖłŹ¾£¬ŌŚ²£Į§¹ÜĮ½¶ĖĶ¬Ź±µĪ¼ÓµČĮæÅØ°±Ė®ŗĶÅØŃĪĖįŗó£¬ŃøĖŁ·ā±ÕĮ½¶Ė”£Ņ»¶ĪŹ±¼äŗ󣬹Ū²ģµ½ŌŚŹż×Ö7Ī»ÖĆŹ×ĻČ²śÉś°×ŃĢ”£ŹŌ½āŹĶ°×ŃĢƻӊŌŚ²£Į§¹ÜÖŠ¼äŹ×ĻČ²śÉśµÄŌŅņ£ŗ__________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé²Ł×÷ÕżČ·µÄŹĒ
A. ĪÅĘųĢåĘųĪ¶ B. ŠæĮ£·ÅČėŹŌ¹Ü
B. ŠæĮ£·ÅČėŹŌ¹Ü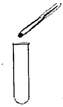 C. ¼ÓČČŅŗĢå
C. ¼ÓČČŅŗĢå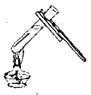 D. µćČ¼¾Ę¾«
D. µćČ¼¾Ę¾«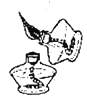
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»Æ·Ź³§Šč“óĮ涞Ńõ»ÆĢ¼Éś²ś»Æ·Ź£¬Óū¹ŗ½ųŅ»ÅśŹÆ»ŅŹÆ(ĘäÖŠŌÓÖŹ²»²Ī¼ÓČĪŗĪ·“Ó¦)£¬³§¼Ņµ½²śµŲȔѳ·ÖĪöŅŌČ·¶Ø¼Ūøń”£ĖūĆĒȔѳ2g£¬²¢°Ń20 gĻ”ŃĪĖį·ÖĖÄ“Ī¼ÓČė£¬³ä·Ö·“Ó¦ŗó£¬Ćæ“ĪŹ£Óą¹ĢĢåÖŹĮæ¼ūĻĀ±ķ:

(1)2gŹÆ»ŅŹÆѳʷ֊ŗ¬ÓŠŌÓÖŹµÄÖŹĮæŹĒ___________æĖ”£ŹÆ»ŅŹÆѳʷ֊Ģ¼ĖįøʵÄÖŹĮæ·ÖŹżŹĒ___________ (ÓĆ°Ł·ÖŹż±ķŹ¾)”£
(2)1000 kgÕāÖÖŹÆ»ŅŹÆ³ä·ÖģŃÉÕŗó£¬æɵƶžŃõ»ÆĢ¼µÄÖŹĮæŹĒ¶ąÉŁ___________?(Š“³ö¾ßĢåµÄ¼ĘĖć¹ż³Ģ) (ģŃÉÕŹÆ»ŅŹÆµÄ»Æѧ·½³ĢŹ½ĪŖ![]() )
)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜŌ“ĄūÓĆÓėÉē»įæɳ֊ų·¢Õ¹ĆÜĒŠĻą¹Ų£¬ŌĶĮ²¢Ķź³ÉĻĀĆęĢīæÕ”£
£Ø1£©2017Äź5ŌĀ18ČÕ£¬ÖŠ¹śÄĻŗ£”°æÉČ¼±ł”±ŹŌ²É³É¹¦£¬±źÖ¾×ÅĪŅ¹ś³ÉĪŖČ«ĒņµŚŅ»øöŌŚøĆĮģÓņŹµĻÖĮ¬ŠųĪČ¶Ø²śĘųµÄ¹ś¼Ņ”£æÉČ¼±ł±»æĘѧ¼ŅÓžĪŖ”°21ŹĄ¼ĶÄÜŌ“”±£¬æÉČ¼±łÖŠ£¬Ė®·Ö×ÓŠĪ³ÉŅ»ÖÖæÕ¼äĮż×“½į¹¹£¬¼×ĶéŗĶÉŁĮæµŖĘų”¢¶žŃõ»ÆĢ¼µČ·Ö×ÓĢīČėĮżÄŚµÄæÕĻ¶ÖŠ£¬ĪŽ¹Ģ¶ØµÄ×é³É£¬Ņņ“ĖæÉČ¼±łŹōÓŚ_____£ØĢī”°“æ¾»Īļ”±»ņ”°»ģŗĻĪļ”±£©£¬ĒėŠ“³öæÉČ¼±łÖŠÖ÷ŅŖ³É·Ö£ØCH4£©Č¼ÉյĻÆѧ·½³ĢŹ½_____”£
£Ø2£©¼×Ķé²»½öŹĒÖŲŅŖµÄČ¼ĮĻ£¬Ķ¬Ź±Ņ²ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ČēĶ¼ŹĒŅŌ¼×ĶéĪŖŌĮĻ£¬Ņ»¶ØĢõ¼žĻĀÖĘČ”Ä³ŅŗĢåČ¼ĮĻµÄĪ¢¹Ū¹ż³ĢŹ¾ŅāĶ¼”£
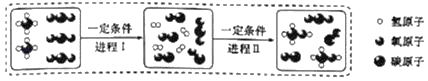
ÓÉ“ĖµĆ³ö£ŗ½ų³ĢIÉś³ÉĪļÖŠµ„ÖŹµÄ»ÆѧŹ½ĪŖ_____£¬½ų³Ģ¢ņ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com