
| A. | 是氧化物 | |
| B. | 氧元素的质量分数计算式为$\frac{6}{176}$×100% | |
| C. | 每个分子中含有20个原子 | |
| D. | 碳、氢、氧三种元素的质量比3:4:3 |
分析 A、根据氧化物的概念:氧化物是只含有两种元素且其中一种元素是氧元素的化合物,据此进行分析判断.
B、根据化合物中某元素的质量分数公式进行分析判断.
C、根据维生素C的微观构成进行分析判断.
D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答 解:A、维生素C是由碳、氢、氧三种元素组成的,不属于氧化物,故选项说法错误.
B、维生素C中氧元素的质量分数为:$\frac{16×6}{12×6+1×8+16×6}$×100%=$\frac{16×6}{176}$×100%,故选项说法错误.
C、维生素C是由维生素C分子构成的,1个维生素C分子是由6个碳原子、8个氢原子和6个氧原子构成的,1个维生素C分子中有20个原子,故选项说法正确.
D、维生素C中,C、H、O三种元素的质量比为(12×6):(1×8):(16×6)=9:1:12,故选项说法错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:解答题
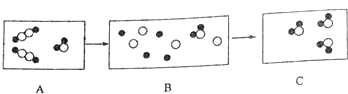 如图用●代表氢原子,〇代表氧子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下:
如图用●代表氢原子,〇代表氧子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
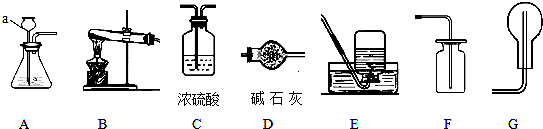
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验现象 | 结论与化学方程式 |
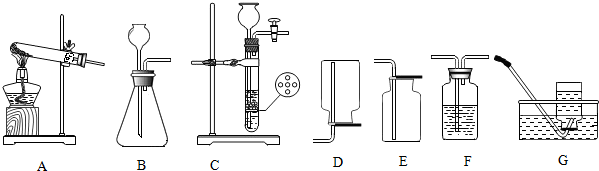
| A中出现黑色固体;B中澄清石灰水变浑浊;D中溶液逐渐变为墨绿色;F中烧杯内壁出现无色液滴. | B中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;装置E中药品的作用是除去气体中混有的水蒸气;收集的气体样品中一定含有H2S、CO2、CH4、O2. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
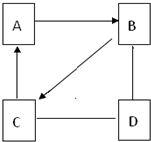 A、B、C、D是初中化学常见的物质,它们分别属于氧化物、酸、碱或盐中的一种,相互反应的关系如图(“-”表示相连的两种物质能发生化学反应,“→”表示转化关系,部分反应物或生成物省略).其中A、B、C含有两种相同元素,B可用于改良酸性土壤.请按要求回答下列问题:
A、B、C、D是初中化学常见的物质,它们分别属于氧化物、酸、碱或盐中的一种,相互反应的关系如图(“-”表示相连的两种物质能发生化学反应,“→”表示转化关系,部分反应物或生成物省略).其中A、B、C含有两种相同元素,B可用于改良酸性土壤.请按要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,加水溶解,往上层溶液中滴加无色酚酞 | 溶液显红色 | 变质的熟石灰中仍含氢氧化钙 |
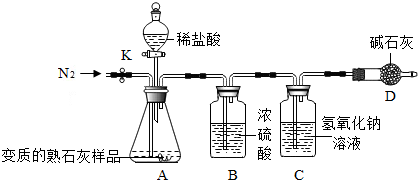
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 熟石灰可用来做建筑材料以及中和酸性土壤 | |
| B. | 用水灭火的原理是降低了可燃物的着火点 | |
| C. | 用C、H2、CO都可以将CuO还原成Cu | |
| D. | 燃烧和缓慢氧化都是放热反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com