
【题目】下图中A、B、C、D是四种常见的物质。其中,A是胃酸的主要成分,B为最轻的气体,C属于盐类,是用小苏打治疗胃酸过多症时发生反应的生成物之一,D的溶液呈黄色。
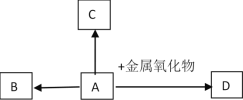
(1)C物质的化学式是__________。
(2)写出符合下列转化的化学反应方程式:
A→B:____________________________(只写一个)
A→D:_______________________________________。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E分别是稀盐酸、氢氧化钠溶液、硫酸铜溶液 、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“------”两端的物质在一定条件下可以反应。
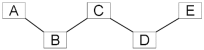
请回答:
(1)E的化学式为___________,该物质属于_______(填:氧化物、酸、碱、盐)。
(2)若F为初中化学常见金属,且能与E反应。则F的化学式为_______,写出F 与E反应的化学方程式:_________________,该反应属于_________(填写基本反应类型)。
(3)若B、C、D、E都不变,五种物质之间的关系也不变,A还可能是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A﹣F表示初中化学常见的物质,它们之间的转化关系如图所示。

若B是一种金属,在空气中燃烧时,会发出耀眼的白光。D是一种红色单质,F是相对分子质量最小的一种气体。
(1)反应①的化学方程式____________________;
(2)反应②基本反应类型为__________;
若A、B、C表示不同类别的化合物,C、E是同类别化合物,E在常温下是一种无色液体,A溶液可以帮助消化,也可以用来除锈,A还能与F发生反应。
(3)写出E的化学式:_____________;C的化学式为:________________;
(4)写出一个符合题意的A与B反应的化学方程式:______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸和碱是初中化学重要的化合物
⑴将①浓盐酸、②浓硫酸、③NaOH 溶液、④Ca(OH)2 溶液、⑤NaCl 溶液分别敞口放置在空气 中,一段时间后,溶液质量增加的是______(填序号).
⑵欲将 50g 溶质质量质量分数为 98%的浓硫酸稀释成 19.6%的稀盐酸,需要加水_____g,请 简述稀释浓硫酸的正确操作.____________
⑶用 NaOH 固体配制 50g 质量分数为 10%的 NaOH 溶液制作“叶脉书签”,所需的玻璃仪器 有___________,量取水时若仰视读数,会使得到的溶液中溶质质量分数____________(填“偏大”、“偏小”或“不变”)
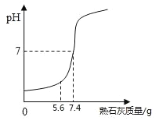
⑷为中和实验后废液中含有的盐酸,取 100g 废液向其中加入熟石灰,反应过程中溶液的 pH 随加入熟石灰质量的变化关系如图所示.
①请根据图示计算废液中盐酸的质量分数____________.
②当加入 5.6g 熟石灰时,溶液中的溶质有______,若改用 7.4g 氢氧化钠与相同量的废液反 应,反应后所得溶液的 pH______7(填“>”,“<”或“=”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示的溶解度曲线,判断下列说法中不正确的是
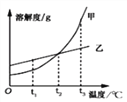
A. t1℃时,甲物质的溶解度小于乙物质的溶解度
B. t2℃时,相等质量的甲、乙两物质的饱和溶液中,所含溶质质量相等
C. 当甲物质中混有少量乙物质时,可采用蒸发结晶的方法,提纯甲物质
D. t3℃时,将等质量的甲、乙两物质配成饱和溶液,需要的水质量:甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)是一种新型吸波隐形材料中的增强剂。
(查阅资料)(1) MgCO3·nH2O微溶于水;
(2) MgCO3·nH2O在230℃时开始失去结晶水, 400℃以上时开始分解生成三种氧化物。
I.合成碳酸镁晶须
步骤:①配制一定溶度的MgSO4溶液和NH4HCO3溶液;②量取一定量的NH4HCO3溶液于容器中,搅拌并逐滴加入MgSO4溶液,控制温度50℃,反应一段时间;③用氨水调节溶液pH至9.5,放置1h后,过滤、洗涤、干燥得碳酸镁晶须产品。
(1)步骤①配制一定溶质质量分数的MgSO4溶液所需要的玻璃仪器有烧杯、胶头滴管、玻璃棒、______________;
(2)步骤②反应的温度控制在50℃,较好的加热方法是__________;
(3)氨水、硫酸镁、碳酸氢铵三者反应,除生成MgCO3·nH2O沉淀外,同时生成的产物还有______________;
(4)检验沉淀已洗涤干净的方法是:取最后一次洗涤的滤液,滴入_________,若无沉淀说明已洗涤干净。
(5)干燥得碳酸镁晶须产品温度不能过高,目的是______________。
II.测定产品MgCO3.nH2O中的n值
(方案一)将碳酸镁晶须放入A装置中加热(仪器和装置如下图所示),回答下列问题:
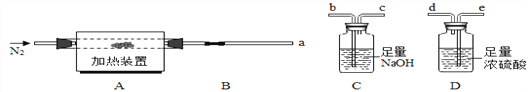
(6)上述装置的连接顺序为_____(按气流方向,用接口字母表示),其中B处的长玻璃导管的作用是__________,C装置的作用是__________。
(7)加热前先通入N2排尽装置中的空气,然后称取C、D的初始质量。再次连接好装置,边加热边通入N2,此时通入N2的作用是_____________。
(8)若B装置中无残留物。装置C反应前后质量差为m1,装置D反应前后质量差m2 。根据以上实验数据,确测定n值, n=___(用含m1、m2的代数式表示)。
(9)有同学提出上述连接好的装置仍不够完善。需要在D装置的后面连接下图装置,目的是________________,否则测得n值会________(“偏大”、“偏小”、“无影响”) 。
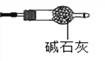
(方案二)
称量100g碳酸镁晶须放入如下图所示的广口瓶中,加入水,滴入稀硫酸与晶须反应,生成的CO2被过量NaOH溶液吸收,在室温下反应4~5h,反应后期将温度升到30℃,最后,烧杯中的溶液加入已知浓度的盐酸恰好完全反应,测得CO2的总量;重复上述操作2次。
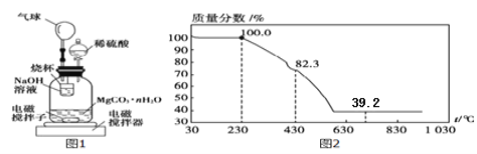
(10)氢氧化钠吸收二氧化碳的化学反应方程式____________________;
(11)图中气球的作用是__________________;
(12)上述反应后期要升温到30℃,主要目的是______________;
(13)设3次实验测得每100 g碳酸镁晶须与稀硫酸反应产生的CO2平均值为ag,则n值为_______(用含a的代数式表示);
(14)称取100g上述晶须产品进行热重分析,热重曲线如图2,则该条件下合成的晶须中,n=_______(写出过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是在分子、原子的层次上研究物质的性质、组成、结构与变化规律的科学。下图是某化学反应的微观示意图,下列说法正确的是
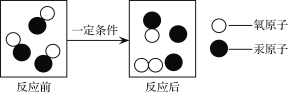
A. 反应前后分子的个数不变 B. 生成物有三种
C. 反应前后汞原子和氧原子的个数不变 D. ![]() 是保持氧气化学性质的最小粒子
是保持氧气化学性质的最小粒子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烧杯中盛有MgSO4和HCl的混合溶液100.0g,向其中逐滴滴加Ba(OH)2溶液,产生沉淀的质量与滴加的溶液质量关系如图所示。
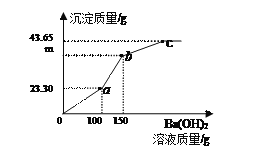
下列说法正确的是
A. a点对应溶液中只有1种溶质
B. b~c段只发生1个反应
C. Ba(OH)2溶液的溶质质量分数约为13.7%
D. m=37.85
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com