


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:不详 题型:实验题
| | 实验操作 | 实验现象 | 实验结论 |
| 猜 想 一 | ________________________________ ________________________________。 | _______________。 | 工业盐溶液显碱性,会造成道路两旁的土壤盐碱化。 |
| 猜想 二 | 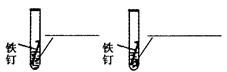 实验① 实验② (请将液体名称填在上面的横线上) | 实验①:6—7天后明显生锈。 实验②: 2—3天后明显生锈。 | __________________ __________________ ________________。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
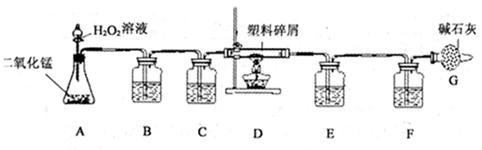
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

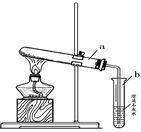
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
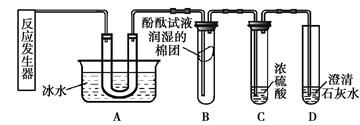
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
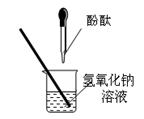
| 实验步骤 | 实验目的 | 现象结论 |
| ①用煮沸过的蒸馏水配制某氢氧化钠溶液。 | 。 | 溶液先变成红色,一会儿红色又消失。 丙同学的猜想不正确。 |
| ②取少量上述氢氧化钠溶液,滴入酚酞,然后在上方滴一些植物油。 | 。 |
| 实验方法 | 观察到的现象和结论 |
| 方案一:分别配制不同质量分数的氢氧化钠溶液,然后各取少量并滴加2滴酚酞溶液。 | 质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明 。 |
| 方案二: 。 | 出现红色且不褪去,结论同上。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
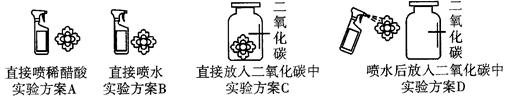
| 猜想 | 实验方案 | 实验现象 | 结论 |
| 可能是CO2使石蕊变红 | C | 小花不变色 | |
| | B | 小花不变色 | 猜想错误 |
| 可能是CO2和水发生反应的生成物使石蕊变红 | | | 猜想正确 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
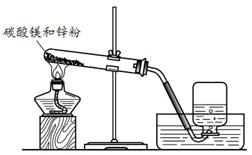
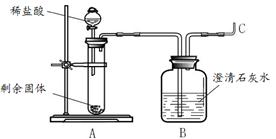
| 序号 | 实验操作 | 实验现象 |
| ① | 收集两瓶气体,盖好玻璃片。向其中一瓶迅速倒入少量澄清石灰水,盖好振荡。 | 无明显现象。 |
| ② | 将另一瓶气体点燃,待火焰熄灭后,迅速倒入少量澄清石灰水,盖好振荡。 | 气体安静燃烧,火焰呈蓝色,澄清石灰水变浑浊。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com