
| A. | 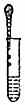 滴加液体 | B. | 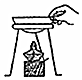 移走蒸发皿 | C. |  收集氧气 | D. |  闻药品气味 |
分析 A、根据使用胶头滴管滴加少量液体的方法进行分析判断.
B、根据蒸发操作的注意事项进行分析判断.
C、根据图中装置用排水法收集气体时,长导管是出水管,进行分析判断.
D、根据闻气体的气味时的方法(招气入鼻法)进行分析判断.
解答 解:A、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误.
B、正在加热的蒸发皿温度较高,为防止烫伤手,不能用手直接拿热的蒸发皿,应用坩埚钳夹取,图中所示操作错误.
C、氧气不易溶于水,用图中装置收集氧气时,长导管是出水管,短导管是进气管,图中所示装置错误.
D、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,图中所示操作正确.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 谷氨酸钠中含有5种元素 | |
| B. | 谷氨酸钠中钠元素的质量分数为13.6% | |
| C. | 20℃时100g水可配制成171.7g谷氨酸钠的饱和溶液 | |
| D. | 熔点232℃为化学性质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用水鉴别MgCl2固体和Mg(OH)2固体 | |
| B. | 用燃着的木条鉴别CO气体和CH4气体 | |
| C. | 用Ca(OH)2鉴别化肥NH4Cl和NH4NO3 | |
| D. | 用AgNO3溶液鉴别KCl溶液和K2CO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
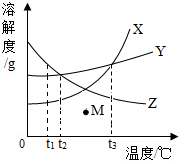 如图是X、Y、Z三种物质的溶解度曲线.
如图是X、Y、Z三种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A、探究二氧化锰对反应速率的影响 | B、探究铁生锈与水有关 | C、探究质量守恒定律 | D、测定空气中氧气的含量 |
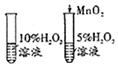 | 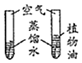 | 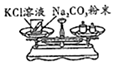 | 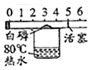 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
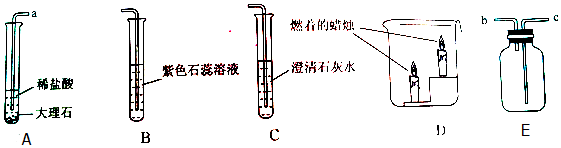
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
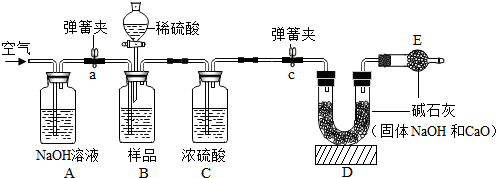
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com