
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 |  | 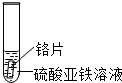 | 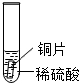 |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面先变灰黑后变银白,溶液由浅绿色逐渐变成为蓝色 | 无明显现象 |
分析 (1)在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此根据能否发生反应,可确定三种金属活动性由强到弱的顺序.
(2)根据金属的表面可能有与氧气反应生成的氧化物或污物,进行分析解答.
解答 解:(1)铁与稀硫酸反应,铁片表面产生气泡较慢,溶液变为浅绿色,说明铁的金属活动性比氢强;将铬片插入硫酸铜溶液中,铬片表面先变灰黑后变银白,溶液由浅绿色逐渐变成为蓝色,说明铬能与硫酸亚铁溶液反应,即铬的金属活动性比铁强;铜的位置排在氢的后面,不能稀硫酸反应,会观察到无明显现象.小聪得到的三种金属活动性强弱顺序是Cr>Fe>Cu.
(2)金属的表面可能有与氧气反应生成的氧化物或污物,用砂纸打磨铁丝和银丝,其目的是除去铁丝和银丝表面的氧化物或污物.
故答案为:无明显现象;(1)Cr>Fe>Cu;(2)除去金属表面的氧化膜(合理即可).
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 钠是一种非常活泼的金属.它可以和冷水直接反应生成氢气,(钠+水→氢氧化钠+氢气,)但是它与煤油不会发生反应.把一小块银白色的金属钠投入盛有蒸馏水的烧杯中,如图所示,可以看到钠浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠和生成的氢气都发生燃烧.如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和
钠是一种非常活泼的金属.它可以和冷水直接反应生成氢气,(钠+水→氢氧化钠+氢气,)但是它与煤油不会发生反应.把一小块银白色的金属钠投入盛有蒸馏水的烧杯中,如图所示,可以看到钠浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠和生成的氢气都发生燃烧.如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
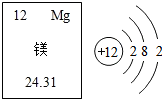 打造更完美的电动汽车,镁电池或将取代锂电池成新一代霸主.(1)元素的相对原子质量为24.31;
打造更完美的电动汽车,镁电池或将取代锂电池成新一代霸主.(1)元素的相对原子质量为24.31;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 坚决取缔马路烧烤 | B. | 开发太阳能等新型能源 | ||
| C. | 提倡使用一次性餐具 | D. | 大力发展公共交通 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用盐酸除去铁锈 Fe2O3+6HCl=3FeCl2+3H2O 复分解反应 | |
| B. | 用木炭还原氧化铜 C+CuO$\frac{\underline{\;加热\;}}{\;}$CO2+Cu 置换反应 | |
| C. | 铁丝在空气中燃烧 3Fe+4O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 化合反应 | |
| D. | 实验室制二氧化碳 CaCO3+2HCl=CaCl2+H2O+CO2↑ 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是需配制的硫酸钠溶液的标签,请计算(整个过程中可溶物完全溶解):
如图是需配制的硫酸钠溶液的标签,请计算(整个过程中可溶物完全溶解):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com