
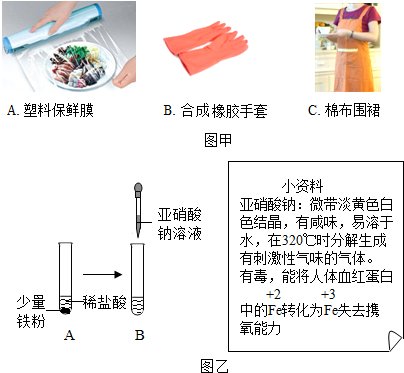
分析 根据已有的人体所需的营养素、洗涤剂的作用、金属铁与盐酸反应的实验现象以及根据溶液的计算进行分析解答即可.
解答 解:(1)①棉布围裙是用天然材料制成的,故填:C;
②还缺少的营养素是维生素,故需要补充的食物是黄瓜,故填:A;
③加碘食盐中的“碘”是指碘元素,故填:元素;
④洗洁精对油污具有乳化作用,故填:乳化;
⑤迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,说明可燃物充分燃烧需要与氧气充分接触,故填:与氧气充分接触;
(2)①500g30%的亚硝酸钠溶液含有亚硝酸钠的质量为:500g×30%=150g=15000mg,亚硝酸钠的最高添加标准为150mg/kg,故至少可以用于生产肉灌肠1000kg,故填:1000;
②铁能与盐酸反应生产氯化亚铁和氢气,加入亚硝酸钠能观察到溶液变黄,说明亚硝酸钠能将亚铁离子转化为铁离子,对人体有毒,故填:铁粉逐渐溶解有大量气泡,溶液变成浅绿色;Fe+2HCl═FeCl2+H2↑;亚硝酸钠能将+2价的亚铁变成+3价铁,对人是有毒的;
③亚硝酸钠加热分解产生的有毒气体是二氧化氮,故填:A.
点评 本题考查的是化学与生活的知识,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:实验探究题
 如图表示几种常见物质之间的转化关系,实现或虚线相连的两种物质之间能够发生反应,箭头表示一种物质能向另一种物质转化.已知A、C为黑色粉末,B为单质,A与D的反应早在西汉时期书籍中就有记载:“曾青得铁则化为铜”,F与G的反应时大自然应用太阳能最成功的范例,A、B、G三种物质可发生反应,生成物的主要成分是红棕色的E.请完成下列内容:
如图表示几种常见物质之间的转化关系,实现或虚线相连的两种物质之间能够发生反应,箭头表示一种物质能向另一种物质转化.已知A、C为黑色粉末,B为单质,A与D的反应早在西汉时期书籍中就有记载:“曾青得铁则化为铜”,F与G的反应时大自然应用太阳能最成功的范例,A、B、G三种物质可发生反应,生成物的主要成分是红棕色的E.请完成下列内容:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是A、B两种物质的溶解度曲线,下列说法正确的是( )
如图是A、B两种物质的溶解度曲线,下列说法正确的是( )| A. | T2℃时,A溶液与B溶液的溶质质量分数一定相等 | |
| B. | 任意温度下,固体A的溶解度一定大于B的溶解度 | |
| C. | 将B的饱和溶液降低温度,溶质质量分数一定减小 | |
| D. | 若A中混有少量B,可用蒸发溶剂的方法进行提纯 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是有关氢氧化钠的性质实验,请简要描述实验①②可能出现的现象并从微观角度解释实验②的反应实质;
如图是有关氢氧化钠的性质实验,请简要描述实验①②可能出现的现象并从微观角度解释实验②的反应实质;查看答案和解析>>
科目:初中化学 来源: 题型:解答题
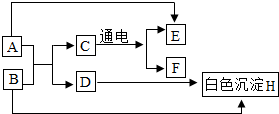 A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.请回答:
A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 分组 | 胃液的pH | 受检患者人数 | 胃液中检出病菌的人数及比例 |
| A | ≤2.0 | 7 | 0 |
| B | 2.0~4.0 | 13 | 3(23.1%) |
| C | 4.0~6.0 | 26 | 17(65.4%) |
| D | >6.0 | 53 | 45(84.9%) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com