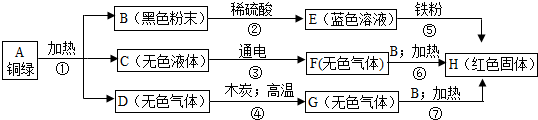
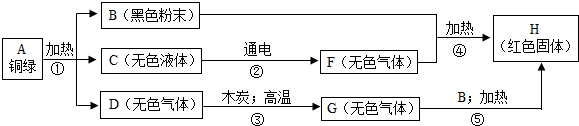
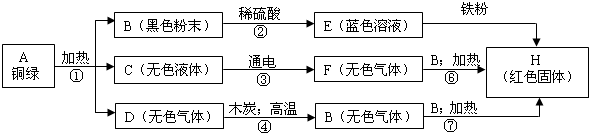
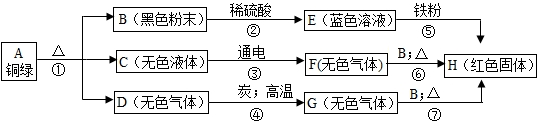
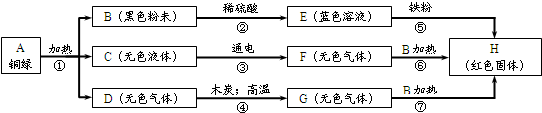
解:(1)E中一定含有铜离子,蓝色溶液E和铁反应生成红色固体H,则H为铜,蓝色溶液E为硫酸铜溶液,黑色粉末B和稀硫酸反应生成蓝色溶液E,则黑色粉末B为氧化铜,无色液体C在通电条件下能分解,则C为水,G和氧化铜加热能生成铜,说明G具有还原性,具有还原性的气体一般是氢气和一氧化碳,G是由D和木炭高温反应生成的,G中含有碳元素,G为一氧化碳,则D为二氧化碳;
(2)湿发冶铜的原理是Fe+CuSO
4═FeSO
4+Cu,所以该原理与⑤所示的反应非常相似;
(3)③为无色液体C在通电条件下能发生反应,可知无色液体C为水,化学方程式为 2H
2O

2H
2↑+O
2↑;
故答案为:(1)CuO;(2)⑤;Fe+CuSO
4═FeSO
4+Cu;(3)2H
2O

2H
2↑+O
2↑;
分析:首先找突破口,从框图中看,B为黑色粉末,初中学过的黑色粉末有木炭、铁粉、氧化铜,E为蓝色溶液、H为红色固体,E+铁→H,推测H为Cu,B为CuO,则F、G为还原性气体,初中学过的还原性气体只有H
2和CO,再根据C通电得F,推出F为H
2、G为CO,进一步推出C为水,D为二氧化碳,此题即可迎刃而解.
点评:根据一些物质特殊的物理或化学性质即可确定该物质,找到解答的突破点,然后根据突破点逐步确定每种物质.本题的突破点就是物质的颜色,抓住这点,即可解答.

 2H2↑+O2↑;
2H2↑+O2↑; 2H2↑+O2↑;
2H2↑+O2↑;