
分析 (1)食品、药品、营养品、矿泉水等物质中的“钙”等不是强调以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(2)根据地壳中含量最多的前五种元素和金属元素的判断方法考虑;海水中含量最高的金属元素是钠
(3)根据金属的物理性质进行分析;
(4)依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式;
(5)赤铁矿的主要成分是氧化铁,在高温的条件下能被一氧化碳还原;
解答 解:(1)高钙豆奶粉的“钙”指的是钙元素,
(2)地壳中含量最多的前五种元素:氧、硅、铝、铁、钙,汉字中带钅字旁(汞和金除外)的属于金属元素,所以地壳中含量最多的金属元素是Al.海水中含量最高的金属离子是Na+;
(3)铝可制成蒸锅,主要利用铝的延展性和导热性;
(4)反应物为氢氧化铝和盐酸,生成物为氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O;
(5)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,其化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
故答案为:(1)元素(2)Al;Na+;
(3)导热(4)Al(OH)3+3HCl═AlCl3+3H2O;
(5)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
点评 此题考查知识点较多,但属于基础性知识的考查,平时一定要注意知识的积累.


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:初中化学 来源: 题型:解答题
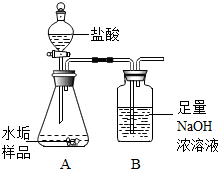 长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:
长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:| 第一次 | 第二次 | 第三次 | 平均值 | |
| B装置增加的质量(g) | 2.17 | 2.22 | 2.21 | 2.20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 加入稀盐酸的质量/g | 0 | 200 |
| 烧杯中物质的质量/g | 25 | 216.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它是混合物 | |
| B. | 它是一种不同于水的新物质 | |
| C. | 它的分子之间有间隔 | |
| D. | 它的一个分子由4个氢原子和2个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
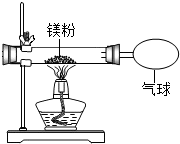 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.| 实验操作 | 实验现象及结论 |
| 将镁条燃烧的产物放在一只试管中,加入少量的蒸馏水,然后将一湿润的红色石蕊试纸放在试管口,观察现象; | 看到红色的石蕊试纸变成蓝色,说明黄色固体为氮化镁 |
| 实验序号 | 实验1 | 实验2 | 实验3 | / |
| 镁条反应的溶液 | NH4Cl | NaCl | Na2S04 | H20 |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡极少 |
| 加热后实验现象 | 气泡明显增多.可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 | 实验现象 | 实验结论 |
| A | 测定溶液pH | 用玻璃棒蘸取待测液滴在用蒸馏水润湿的pH试纸上 | 试纸变为浅红色 | 溶液pH为2 |
| B | 鉴别NaOH和NH4NO3 | 在装有等量水的试管中分别加入a、b固体 | 加a的试管水温升高,加b的试管水温降低 | A是NaOH,b是NH4NO3 |
| C | 验证燃烧是否需要O2 | 做白磷是否燃烧的对比实验 | 前者不燃烧,后者燃烧 | 燃烧需要O2 |
| D | 比较Al、Cu的活泼性 | 将未经打磨的Al条放入CuSO4溶液中 | 无明显现象 | Al的活性炭低于Cu |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com