
碱式碳酸盐广泛应用于工农业生产。
(查阅资料)①碱式碳酸铜可以表示为Cu(OH)2·mCuCO3,是常见的碱式碳酸盐。
②碱式碳酸盐M(OH)2·MCO3不溶于水,与碱式碳酸铜具有相似的化学性质。
③无水硫酸铜是白色粉末,能与水作用生成蓝色固体。
(1)研究小组欲确定某碱式碳酸盐样品M(OH)2·MCO3中金属M的相对原子质量。
(实验装置)
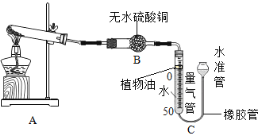
(实验步骤)
①连接装置并检査装置气密性;②准确称量样品的质量;③装药品,调节量气装置两边液面相平,读数;④点燃酒精灯,加热样品至质量不再减少;③冷却到室温;⑥调节量气装置两边液面相平,读数、列式计算。
I.步骤①中检査装置气密性的方法是_____________。
Ⅱ.装置B的作用是________,装置C中植物油的作用是____。
Ⅲ.步骤⑥中调节液面相平的操作是将水准管_____(填“缓慢上移”或“缓慢下移”)。
Ⅳ.若其它操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是_____(填序号)。
a.反应前量气管水面在0刻度处,反应后仰视读数 b.样品未分解完全即停止实验
c.量气管中未加植物油
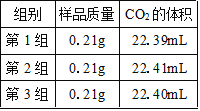
(2)某研究小组仍使用上述装置測定m的值,测得3组数据如表所示。实验测得CO2的体积为__________mL,又已知常温常压下CO2的密度为1.964g/L,据此计算m的值为______(结果保留两位小数)。
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源:广东省惠州市仲恺区2019届九年级下学期中考一模化学试卷 题型:科学探究题
现有一包白色粉末,可能由NH4Cl、Na2CO3、NaHCO3中的一种或几种组成。小莹为了探究其成分,进行了如下实验:
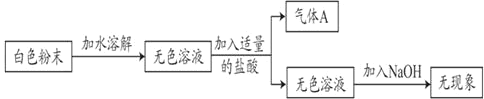
(1)由上述实验可知气体A是_____。
(2)根据上述的实验现象,原白色粉末一定没有_____。
(3)(发现问题)Na2CO3、NaHCO3与盐酸反应,均能产生气体,无法确定固体的成分。
(查阅资料)
①NaHCO3与可溶性的钙盐、钡盐混合没有沉淀产生。
②NaHCO3与足量的Ca(OH)2反应有白色沉淀产生。
(提出猜想)
猜想1:白色粉末只有_____;
猜想2:白色粉末只有Na2CO3;
猜想3:白色粉末是_____。
(实验探究)
小勇为了验证其猜想,取少量的白色粉末放入烧杯中,加水全部溶解后,加入足量的Ca(OH)2溶液,现象是_____,他就认为猜想二正确。小杰认为小勇的结论不正确,理由是_____,
于是他做了进一步的探究:
实验操作 | 现象 | 实验结论 |
取白色粉末于烧杯中,加水溶解,再加入BaCl2溶液充分搅拌,静置 | 若无_____现象 | 猜想_____成立 |
若_____ | 证明白色固体肯定有_____,可能有_____ | |
取10.6g白色粉末于锥形瓶中,加入足量稀盐酸后把生成的气体通入足量的NaOH溶液中,反应完全后称得NaOH溶液增重4.5g | 确认猜想_____成立 |
查看答案和解析>>
科目:初中化学 来源:江苏省扬州市2019届九年级下学期中考一模化学试卷 题型:科学探究题
过氧化钙(CaO2)在生产中具有广泛的应用
(一)过氧化钙的性质与用途
(1)CaO2能与稀盐酸发生复分解反应,反应的化学方程式为_____。
(2)鱼类长途运输的增氧剂的主要成分为CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为_____,Na2O2也能与水反应,原理与CaO2相同,但却不能作为鱼虾运输的供氧剂,请分析可能的原因_____。
(二)过氧化钙晶体的制备
(资料)过氧化钙晶体(CaO2·yH2O),常温为白色,能溶于酸,难溶于酒精。
制备原理:CaCl2+H2O2+NH3+H2O→CaO2·yH2O↓+NH4Cl,装置如下。
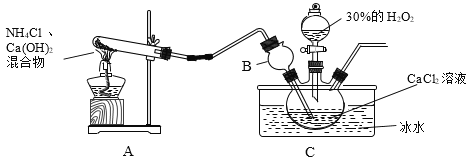
(1)装置A中试管内发生反应的化学方程式为_____。
(2)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ.该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ._____。
(3)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。
①洗涤时采用95%的酒精溶液洗涤的优点是_____。
②检验晶体已洗涤干净的方法为_____。
(三)过氧化钙晶体组成的测定
称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水),
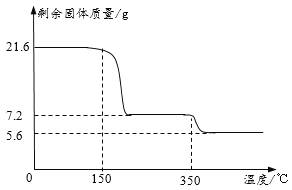
(1)0—150℃质量不发生改变的原因是_____。
(2)根据如图可知y=_____。(写出计算过程)
(3)350℃时发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源:江苏省扬州市2019届九年级下学期中考一模化学试卷 题型:单选题
以甲为原料得到丙反应的微观过程如下:
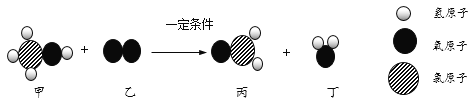
下列说法正确的是
A. 该反应为置换反应 B. 转化中甲和乙的分子个数之比为1∶1
C. 甲中氧元素的质量分数大于丙 D. 反应中一定有元素化合价发生改变
查看答案和解析>>
科目:初中化学 来源:江苏省扬州市2019届九年级下学期中考一模化学试卷 题型:单选题
下列化学用语正确的是( )
A. 小苏打﹣Na2CO3 B. 铝离子﹣Al2+
C. 二氧化氯﹣ClO2 D. 氯酸钾﹣KCl
查看答案和解析>>
科目:初中化学 来源:江苏省常州市部分学校2019届九年级下学期中考模拟化学试卷 题型:填空题
如图所示是简易净水器。
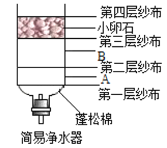
(1)为更好提升净水效果,B层放置的材料最好是_________(选填“活性炭”或“石英砂”)。
(2)该简易净水器__________(选填“能”或“不能”)将硬水变成软水。检验一份水样是硬水还是软水,最常用的试剂是_____________。生活中将硬水变成软水的方法是_____。
(3)节约用水是每个公民的义务,下列用水方式应该提倡的是____________(填字母序号)。
a用漱口杯接水刷牙 b不间断地边流水边洗衣
c用淘米水、洗菜水浇花、冲厕所 d用喷灌、滴灌的方法浇灌农田和园林
查看答案和解析>>
科目:初中化学 来源:江苏省常州市部分学校2019届九年级下学期中考模拟化学试卷 题型:单选题
下列离子能在pH=13的水溶液中大量共存的是
A. K+、SO42-、NH4+ B. K+、Cu2+、NO3-
C. Cl-、Na+、CO32- D. Ca2+、CO32-、Na+
查看答案和解析>>
科目:初中化学 来源:福建省漳州市平和县2019届九年级下学期中考二模化学试卷 题型:科学探究题
某废液 M 可能含有 NaCl、NaOH、Na2CO3、Na2SO4 中的一种或几种,为确定其成分进行实验探究。
(资料信息)
物质 | NaCl | NaOH | Na2CO3 | Na2SO4 |
常温下溶液的 pH | 7 | 13 | 11 | 7 |
(探究过程)
实验步骤 | 实验现象 | 实验结论 |
步骤一:取适量废液 M 于试管 中,滴加无色酚酞试液。 | 无色酚酞变红色 | 有同学认为废液 M 中一定含有 NaOH。 请你对该结论作出判断并说明理由_____。 |
步骤二:重新取适量废液 M 于 试管中,滴加足量的稀盐酸。 | 有气泡产生,产生的气体 能使澄清石灰水变浑浊 | 废液 M 中一定含有______。判断依据 是_____(用化学方程式表示) |
步骤三:再重新取适量废液 M 于试管中,先滴加过量的稀硝酸,再滴加过量的_____溶液,静置。 | 有白色沉淀 | 由步骤三、步骤四可知:废液 M 中一定有_____。 |
步骤四:取步骤三中的上层清 液,滴加过量的_____溶液。 | 有白色沉淀 |
(实验反思)步骤三空中滴加的溶液一定要过量的原因是_____。
查看答案和解析>>
科目:初中化学 来源:广东省茂名市九校2019届九年级下学期期中考试化学试卷 题型:单选题
下列过程属于化学变化的是( )
A. 干冰升华
B. 镁条放置于空气中,表面有一层灰白色的膜
C. 活性炭吸附毒气
D. 石油蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com