用“>”、“=”、“<”填空.
(1)V1mL水和 V2mL酒精混合得混合液体积 V3mL,则V1+V2 V3.
(2)20℃时,100g Ca(OH)2 饱和溶液中溶质质量分数为a1%,60℃时200gCa(OH)2 饱和溶液中溶质质量分数为a2%,则a1% a2%.
(3)质量为m g的铁片插入某硫酸铜溶液中,一段时间后取出附有铜的铁片,称得其质量为n g,则m n.
【答案】
分析:(1)根据分子之间有间隔来分析液体混合时体积的变化;
(2)根据温度对饱和溶液的溶解度的影响来分析溶质的质量分数的变化;
(3)根据溶液质量的变化来分析固体的质量的变化,利用差量法来解答.
解答:解:(1)因分子之间有间隔,当V
1mL水和 V
2mL酒精混合时,分子之间的间隔发生变化,使混合溶液的体积小于水和酒精的体积之和,故答案为:>;
(2)因溶液为 Ca(OH)
2 饱和溶液,随温度的升高溶解度在减小,由w%=
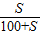
×100%,则60℃时溶解度小时溶质质量分数a
2%就小,故答案为:>;
(3)根据铁和硫酸铜溶液反应的化学方程式Fe+CuSO
4═FeSO
4+Cu可知,
Fe+CuSO
4═FeSO
4+Cu△m
56 64 8
显然每56份质量的铁与溶液反应,溶液就减轻8份质量,则固体的质量就增加,
即n>m,故答案为:<.
点评:本题较容易出现错误,考查的知识点多,注重学生思维严密性的训练,应注意利用体积不能加和、Ca(OH)
2饱和溶液、溶液的质量变化等来解答.

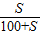 ×100%,则60℃时溶解度小时溶质质量分数a2%就小,故答案为:>;
×100%,则60℃时溶解度小时溶质质量分数a2%就小,故答案为:>;