
【题目】(一)锌锰电池(俗称干电池)在生活中的用量很大,其构造如图所示。

(1)根据右图判断,属于金属材料的是_______。
(2)易溶于水的氯化铵固体中混有难溶物二氧化锰,提纯氯化铵固体的实验步骤是:溶解、_______、结晶。
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如图所示:

已知:Cu+H2O2+H2SO4 △ CuSO4+2H2O
下列说法正确的是_____________。
A.溶液B与溶液F中所含溶质相同 B.过程Ⅱ中发生的反应均为置换反应
C.溶液F比溶液B中含硫酸锌的质量多 D.A~F中含铜、锌两种元素的物质有两种
(二)A~F为初中化学常见物质,它们由H、C 、O、S、Na、Ca中的2~3种元素组成。
(1)A为气体,是常用的灭火剂,则A的化学式为 。
(2)A与B组成元素相同,写出B转化为A的化学方程式 。
(3)C与D两种物质间能发生中和反应,且C的相对分子质量大于D 的相对分子质量,则D的化学式为 。
(4)E常用于改良酸性土壤,F为A与D反应的生成物,则F的俗称为 ;取E与F反应后的溶液,滴加C物质,一段时间后有气体产生,再滴加无色酚酞,溶液仍为无色,此时溶液中的溶质是 (写出所有可能,除酚酞外)。
【答案】(一) (1)铜帽 锌筒(2)过滤(3)BCD(二)(1)CO2(2)2CO+O2点燃2CO2 或
3CO+Fe2O3高温2Fe+3CO2(3)NaOH(4)纯碱或苏打 Na2SO4;Na2SO4、H2SO4
【解析】
试题分析:根据右图判断,属于金属材料的是铜帽 锌筒。易溶于水的氯化铵固体中混有难溶物二氧化锰,提纯氯化铵固体的实验步骤是:溶解、过滤、结晶。过程一中加入过氧化氢,目的是将铜完全转化为硫酸铜,变为溶液,过程二是加入酸将锌变为硫酸锌,过程中发生的反应为置换反应;A~F中, E中含有铜和锌,所以说法正确的是过程Ⅱ中发生的反应均为置换反应;溶液F比溶液B中含硫酸锌的质量多;A~F中含铜、锌两种元素的物质有两种;A为气体,是常用的灭火剂,则A的化学式为CO2。A与B组成元素相同,则说明B是CO,B转化为A的化学方程式2CO+O2点燃2CO2 或3CO+Fe2O3高温2Fe+3CO2。C与D两种物质间能发生中和反应,且C的相对分子质量大于D 的相对分子质量,则D为氢氧化钠,E常用于改良酸性土壤,说明E是氢氧化钙,F为A与D反应的生成物,则F的俗称为纯碱或苏打;取E与F反应后的溶液,滴加C物质,一段时间后有气体产生,再滴加无色酚酞,溶液仍为无色,说明C是一种酸,而且酸过量,因为酚酞不变色,如果酸不足酚酞的颜色是红色,所以此时溶液中的溶质是Na2SO4、H2SO4。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】右图是常见固体物质的溶解度曲线,根据图示回答:

(1)对A物质来说,a点的意义是 。
(2)将t1℃140g A的饱和溶液升温至t2℃时,可用图上
的 点表示,此时溶液是 (填“饱和”或“不饱和”)状态,然后再加入A物质40g,可用曲线上的 点表示。t2℃时A、B、C三种物质饱和溶液的质量分数由大到小的顺序是 。
(3)若将d点温度下A、B、C三种物质的饱和溶液降温至t1℃,没有晶体析出的是 物质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,下图是它们之间的相互转化关系(部分产物略去)。请回答:

(1)写出下列物质的化学式:A. C. E. 。
(2)若G是蓝色溶液则B的化学式是: 。
(3)若I是红褐色沉淀,请写出G + F → I的化学方程式: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】原电池中若用活泼性不同的两种金属作电极时,一般活泼性较强的作负极。现有A、B、C、D四种金属,只有A、C可与稀硫酸反应放出H2且A、C形成原电池时C作负极,D与B的硝酸盐溶液反应可置换出B的单质,则四种金属活泼性由弱到强的顺序是
A.A、C、D、B B.A、B、C、D
C.B、D、A、C D.C、A、D、B
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是
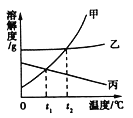
A.t2℃时甲、乙两物质的溶解度相等
B.温度大于t2℃时,甲、乙、丙三种固体物质溶解度的大小关系是甲>乙>丙
C.当甲中混入少量乙时,可用冷却热饱和溶液的方法得到较纯净的甲
D.t2℃时甲、丙两物质的饱和液降温到t1℃时,两者所得溶液的溶质质量的分数一定相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图表示的是KNO3和NaNO3的溶解度曲线。下列说法正确的是

A.T2℃时,KNO3溶液的浓度一定等于NaNO3溶液的浓度
B.T1℃时,在50g水里加入15g KNO3固体,充分溶解,可得到65g溶液
C.T1℃时,往180g NaNO3饱和溶液中加入620g水可配成质量分数为10%的NaNO3溶液
D.若KNO3中混有少量NaNO3,可用蒸发溶剂的方法提纯KNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的食品和饲料添加剂,某补血剂样品【主要成分为硫酸亚铁晶体(FeSO4xH2O)】,某化学兴趣小组对其产生了兴趣并进行了探究:
【探究一】硫酸亚铁晶体(FeSO4xH2O)热分解研究
【查阅资料】
1.无水硫酸铜粉末遇水会变成蓝色的硫酸铜晶体;
2.硫酸亚铁晶体加热时,先失去结晶水,高温会继续分解产生金属氧化物和气态非金属氧化物。
3.二氧化硫能使高锰酸钾溶液褪色。
【进行实验】该兴趣小组同学称取27.8g硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行分析,并利用SDTQ600热分析仪,对硫酸亚铁晶体热分解获得相关数据,绘制成图2所示的关系图,试回答:
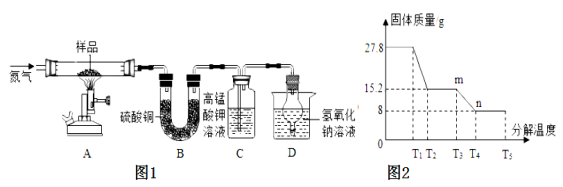
(1)装置B中硫酸铜粉末变蓝,说明产物中有 ,该物质的质量是 g;装置C中高锰酸钾溶液褪色,说明产物中还有 ;硫酸亚铁晶体完全分解后,装置A中的固体呈红棕色,放入足量稀盐酸,固体全部溶解,且得到黄色溶液,则该红棕色固体与稀盐酸反应的化学方程式为 。
(2)D装置中球形干燥管的作用是 。
(3)硫酸亚铁分解生成铁的氧化物和硫的两种氧化物,请写出化学反应方程式 。
(4)根据图2中的数据,请求出FeSO4xH2O中的x= 。(不写过程)
【交流讨论】实验中要持续通入氮气,否则测出的x会 (填“偏大”、“偏小”或“不变”)。
【探究二】补血剂样品中硫酸亚铁的含量:
①取10g补血剂样品研细后溶于40g水中,研细的目的是 ;
②向所配制的溶液中加氯化钡溶液至略过量,使其充分反应;
③过滤,洗涤,干燥,称量所得白色固体的质量为6.99g。
请计算出10g样品中FeSO4的质量分数,写出计算过程。此题2分。
(已知:FeSO4+BaCl2=BaSO4↓+FeCl2,有关相对分子质量:FeSO4—152,BaSO4—233)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据图7中A、B两种固体物质的溶解度曲线,回答下列问题。

(l)在____℃时,A、B两种物质溶解度相同。
(2)t2℃时,100g水中溶解_ gA物质恰好达到饱和,该饱和溶液中溶质的质量分数为_ ___,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水 _ ___g。
(3)将t2℃时A、B两种物质的饱和溶液降温至t1℃(其它条件不变),溶质的质量分数保持不变的是__ _。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如右图是初中化学常用的部分实验仪器,据此回答问题:
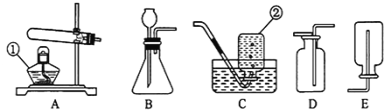
(1)写出标有序号的仪器名称:① , ② ;
(2)用氯酸钾制取氧气若用A装置,应该去掉 。
(3)应选用气体发生装置和收集装置为 (填字母编号)实验中,有同学发现对药品加热一段时间后收集不到氧气,可能的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com