
已知氢在标准状况下的密度为0.0899 g/L,则2.016 g氢气在标准状况下的体积为
[ ]
A.2 L B.11.2 L C.22.4 L D.1.8 L
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:阅读理解

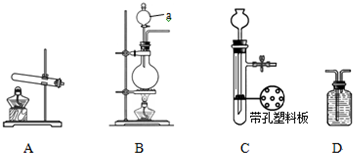
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① (NH4)2SO4+Ca(OH)2═2NH3↑+2H2O+CaSO4 (NH4)2SO4+Ca(OH)2═2NH3↑+2H2O+CaSO4 |
| 乙小组 | ② B B |
浓氨水、氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源:山东省中考真题 题型:实验题

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
含镁3%~5%的镁铝合金是轮船制造、化工生产、机械制造等行业的重要原材料。现有一块质量为w g的镁铝合金,某研究性学习小组欲测定其中镁的质量分数。
【查阅资料】已知铝与NaOH溶液反应生成易溶于水的偏铝酸钠(NaAlO2:)和H2,化学方程式为:2A1+2NaOH+2H2O=2NaAlO2+3H2↑;镁不与NaOH溶液反应。氢氧化铝能与氢氧化钠溶液发生反应生成易溶于水的偏铝酸钠(NaAlO2:)和H2O,化学方程式为:A1(OH)3+NaOH=NaAlO2+2H2O;氢氧化镁不与氢氧化钠溶液反应。
【提出猜想】利用镁铝与酸、铝与碱、氢氧化铝与碱反应的化学性质来测定合金中镁的质量分数。
【设计方案】研究小组设计了不同的实验方案。
方案l:镁铝合金与过量盐酸反应测定生成气体在标准状况下的体积为V1L;
方案2:镁铝合金与过量NaOH溶液充分反应后,过滤、洗涤、干燥、称量剩余固体的质量为w1g;
方案3:镁铝合金与过量盐酸溶液反应后再与过量NaOH溶液反应,过滤、洗涤、干燥、称量沉淀的质量为w2g。
【问题讨论】请你参与研究小组的研究过程,并回答有关问题:
(1)研究小组利用如图所示实验装置,按照方案1进行了实验。
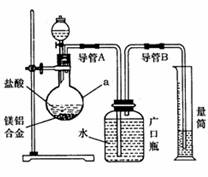
①装置中仪器a的名称是 。
②实验装置中有一处明显错误,请指出
(2)方案2中剩余固体是 ;若按方案2进行实验,测得镁的质量分数为 。
(3)方案3中“过滤”得到的沉淀是 。
(4)某同学又设计了与上述方案原理不同的方案4,也能测得镁的质量分数。请你在横线上填写合适的内容,将该方案补充完整。
方案4:镁铝合金与 反应测定生成气体在标准状况下的体积为V2L。
【方案评价】
(5)在实验方案1-4中,你认为最佳的实验方案是 。
查看答案和解析>>
科目:初中化学 来源:2013年第二十三届“天原杯”全国初中学生化学素质和实验能力竞赛(天津赛区)初赛试卷(解析版) 题型:填空题
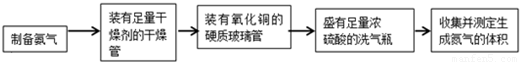
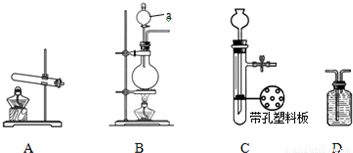
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① |
| 乙小组 | ② | 浓氨水、氢氧化钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com