
硝酸钾的溶解度如表所示,下列有关叙述正确的是( )
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/(g/100 g水) | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
 A.20℃时,可配成50 g 35%的硝酸钾饱和溶液
A.20℃时,可配成50 g 35%的硝酸钾饱和溶液
B.30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者
C.40℃时,50 g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3 g
D.60℃时,50 g硝酸钾饱和溶液中,溶质与溶剂的质量比为11∶21
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
除去下列物质中混有的杂质,所选用的试剂及操作方法正确的是
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| B | CO2 | CO | 通过NaOH溶液,洗气 |
| C | NH3 | H2O | 通过浓硫酸,洗气 |
| D | KCl固体 | KOH固体 | 加入过量的HCl溶液,过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:
工业绿矾(主要成分FeSO4·7H2O),其中所含固体杂质不含铁元素、不溶于水、加热也不分解。用铁的质量分数为18%以上的工业绿矾可生产复印用高档Fe3O4粉。
一、原料工业绿矾中铁的质量分数测定
称取30g硫酸亚铁晶体样品按图1高温加热,使其完全分解,相关数据如图2,对所得产物进行探究,并测定样品中铁的质量分数。
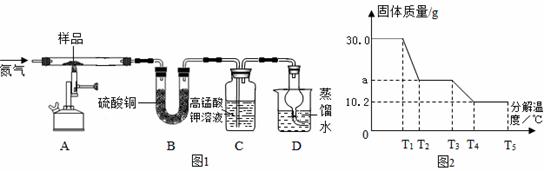
【查阅资料1】绿矾晶体在T1时开始分解,T2时完全失去水,T3时FeSO4开始分解。
(1)实验前,应先 △ 。
(2)装置B中硫酸铜粉末变蓝,说明产物中有 △ ,装置C中高锰酸钾溶液褪色,
说明产物中还有 △ 。
(3)装置A中固体变成红棕色,放入稀盐酸,得黄色溶液,则该红棕色固体是 △ 。
(4)装置D球形干燥管的作用 △ 。
(5)从理论上分析,硫酸亚铁晶体分解还生成SO3 。根据相关数据分析:①图2中T3至T4过程的反应化学方程式 △ ;②样品中铁的质量分数= △ 。
(6)实验中要持续通入氮气,否则测出的铁的质量分数会 △ (填“偏大”、“偏小”或“不变”) 。
。
【查阅资料2】
① 硫酸亚铁在不同温度下的溶解度如下表所示:
| 温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/ g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
②Fe(OH)2易氧化:4 Fe(OH)2 + 2H2O + O2 = 4 Fe(OH)3
③ 获得Fe3O4的反应原理为:Fe(OH)2 + 2Fe(OH)3  Fe3O4 + 4H2O
Fe3O4 + 4H2O
(1)溶解时,用50℃至80℃的热水目的是 △ 。
(2)写出加入适量NaOH溶液时发生反应的化学方程式 △ 。
(3)副产品P的化学式是 △ 。
(4)沉淀M需洗净,检验是否洗净的方法是 △ 。
(5) 若流程中产生的Fe(OH)2和Fe(OH)3的质量比为50∶107,则所得产品是 △ 的Fe3O4(填“纯净”或“不纯净”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
实验中常常要用到氢氧化钠溶液。氢氧化钠溶液暴露于空气中易变 质,变质后的溶液为 (填化学式)溶液;向变质后的溶液中加入氯化钙溶液能够观察到的现象是 ,有关的化学方程式为 。
质,变质后的溶液为 (填化学式)溶液;向变质后的溶液中加入氯化钙溶液能够观察到的现象是 ,有关的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
26.
27.
28.
29.
30.
31.
32.
33.
右图为××钙片商品标签图,请根据标签的有关信息完成
下列各题。
(1) 其主要成分碳酸钙由 种元素组成;
(2) 碳酸钙中钙、碳、氧元素的质量比为 ;
(3) 每片钙片中至少含钙元素  g。
g。
 |
查看答案和解析>>
科目:初中化学 来源: 题型:
氧气在自然界中存在非常广泛,并不断循环转化。请回答以下问题:
(1)下图是自然界中氧的部分循环示意图.从①~⑥中选择序号填空,产生氧气的有______。

(2)铁生锈、动植物的呼吸___________(填“是”或“不是”)缓慢氧化。
(3)2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测
指标,PM2.5是用来监测空气中下列哪项含量的____________(填序号)。
①二氧化碳 ②一氧化碳 ③二氧化硫 ④可吸入颗粒物
(4)下列措施中不能降低空气中PM2.5的是____________(填字母)
a、戴口罩 b、禁止焚烧秸秆 c、植树造林
(5)将沸点不同的气体分离开来,常采用液化分离法。如,控制温度在-183℃时,可将空气中氮气(N2)与氧气(O2)分离。根据下表中物质的沸点判断,要将产物氨气(NH3)与N2、氢气(H2)分离开来,最适宜的温度应该控制在 ℃。
| 物质 | H2 | N2 | O2 | NH3 |
| 沸点 | -252℃ | -195.8℃ | -183℃ | -33.35℃ |
工业上分离液态空气制氧气,该过程属于__________(填“物理”或“化学”)变化。
查看答案和解析>>
科目:初中化学 来源: 题型:
有关水分子变化的叙述正确的是
A.用水壶烧水时,壶盖被顶开,说明水分子的体积在受热时变大了
B.水可以结成冰,说明水分子的化学性质发生改变
C.电解水生成氢气与氧气,说明水分子可以再分解
D.发生化学反应时,构成水分子的原子种类发生改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com