
“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图。下列说法正确的是( )
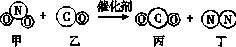
A.生成的丙和丁的分子个数比为1∶1
B.反应 前后,碳和氮的化合价发生了改变
前后,碳和氮的化合价发生了改变
C.反应前后,元素的种类没有改变,原子的个数发生了变化
D.乙和丙的元素组成相同,所以它们的化学性质相同
 学业测评一课一测系列答案
学业测评一课一测系列答案科目:初中化学 来源: 题型:
(NH4)2SO4、NH4NO3、CO(NH2)2是常见的化肥,对提高农作物产量有重要作用。
(1)上述物质中属于有机物的是 ;
(2) NH4NO3中N、H、O三种元素的质量比为 ;
(3)为测定(NH4)2SO4化肥样品中氮元素的质量分数,小民和小青分别按自己设计的方案进行了实验(样品中杂质可溶,且不参与反应)。
方案 1:小民称取13.60g样品,与足量的浓NaOH溶液混合加热,充分反应后,将获得的气体直接用足量的浓硫酸吸收,浓硫酸增重3.91g。
1:小民称取13.60g样品,与足量的浓NaOH溶液混合加热,充分反应后,将获得的气体直接用足量的浓硫酸吸收,浓硫酸增重3.91g。
方案2:小青另取等质量的样品溶于水,向水中加入足量的BaCl2溶液,充分反应后将沉淀过滤、洗涤、干燥,得白色固体23.30g。
①上述不合理的方案是 ;简述理由 。
②选用合理方案计算该(NH4)2SO4化肥样品中氮元素的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
下图表示治理汽车尾气所涉及反应的微观过程。下列说法不正确的是
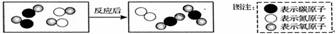
A.图中所示单质的化学式为N2 B.  反应前后无元素化合价改变
反应前后无元素化合价改变
C.图中所示有三种氧化物的分子 D. 反应后分 子个数减少了
子个数减少了
查看答案和解析>>
科目:初中化学 来源: 题型:
 请根据下列装置,回答问题:
请根据下列装置,回答问题:
(1)写出有标号的仪器名称:① △ ,② △ 。
(2)用高锰酸钾制取O2时,选A、D进行实验,写出该反应化学方程式 △ ; 发现水槽中的水变红的原因为 △ ;气体收集完毕时,应先 △ (填A或B)。A.从水中取出导气管 B.熄灭酒精灯
(3)某同学在实验室制二氧化碳气体时,写出该反应化学方程式 △ 。
将气体的发生装置由B改进为F,这样做的优点是 △ 。
(4 )实验室用固体无水醋酸钠和碱石灰混合物加热的方法制取甲烷(甲烷的密度比空气小,且不溶于水)。该实验可选用的发生装置是 △ ,收集装置是 △ 。
)实验室用固体无水醋酸钠和碱石灰混合物加热的方法制取甲烷(甲烷的密度比空气小,且不溶于水)。该实验可选用的发生装置是 △ ,收集装置是 △ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
人体健康离不开化学。下列叙述正确的是( )
A.铁、锌、钙是人体所需的微量元素
B.只要胃液的pH<7,人体就是健康的
C.人体缺少铁元素会引起缺铁性贫血
D.为防止龋齿,应在牙膏中添加大量的氟元素
查看答案和解析>>
科目:初中化学 来源: 题型:
现有X、Y、Z三种金属,分别发生下述反应:Y+ZSO4 YSO4+Z;X在常温下与氧气反应,而Y在高温下才能与氧气反应。则X、Y、Z的金属活动性顺序是( )
YSO4+Z;X在常温下与氧气反应,而Y在高温下才能与氧气反应。则X、Y、Z的金属活动性顺序是( )
A.X>Y>Z B.Y>X>Z C.Z>X>Y D.X>Z>Y
查看答案和解析>>
科目:初中化学 来源: 题型:
17.
18.
19.
如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态。化合物D的水溶液呈浅绿色。
(1) 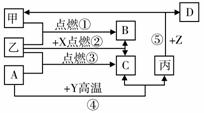 写出有关物质的化学式:X._________;
写出有关物质的化学式:X._________;
(2) 指出反应④在生产实际中的应用:_____________________(举一例说明);
(3) 将A、C两种氧化物区别开来,可使用的一种溶液为__________________(填名称);
(4) 写出下列反应的化学方程式:③ ;⑤ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属.流程如下
其中错误的是
A.固体丙中一定只含银 B.四种金属活动性强弱顺序Zn、X、Cu、Ag
C.固体甲中一定含有Cu 和 Ag,可能含有X D.滤液C中只含有Cu(NO3)2
查看答案和解析>>
科目:初中化学 来源: 题型:
我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献。用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验。
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应。
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳。
[方案一] 样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液。 | 产生白色沉淀 | 反应的化学方程式:
|
(2)分析滴加的CaCl2溶液要过量的原因:___________________;
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤.干燥.称量。利用沉淀物质量计算Na2CO3的质量分数为91%。如果不洗涤沉淀物会造成测定结果大于91%,这是因为 _____ 。
[方案二] 样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计 算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。
算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。
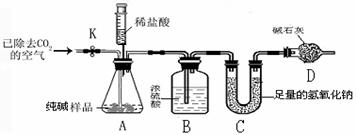
(4) 打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的 ,再接上装置C和D。
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为__________________ 。
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿。根据质量守恒定律,装置_________(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数。若没有装置D,将会使测定结果 ________(选填“偏大”或“偏小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com