
【题目】请运用所学化学知识填空:
(1)拉瓦锡通过实验测得,氧气约占空气体积的________;硫在氧气燃烧会伴随___________色火焰。
(2)从微观视角看,“春雨丽润泽桃花开,微风拂面清香来”说明_________; CH3COOH、HCl等物质的水溶液都能使石蕊溶液变为红色的原因是:它们的溶波中都含有_________(填微粒名称)。
(3)构成硫酸铁的阳离子符号为:_________;甲烷完全燃烧的化学方程式为:___________________。
(4)依据下图回答问题:
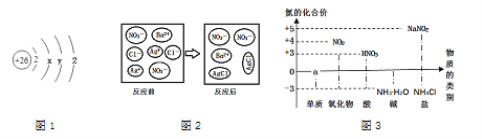
①图1中y的值为________
②另写1个与图2所示微观反应本质相同的化学方程式_____________·
③写出图3中a处的1种物质名称:_____________,其中位置放错的物质有:___________(填化学式)。
【答案】 1/5 蓝紫 构成物质的微粒是不断运动的 氢离子 Fe3+ CH4 + 2O2 ![]() CO2 +2H2O 14 NaCl + AgNO3 = AgCl ↓+ NaNO3 氮气 HNO3、NaNO2
CO2 +2H2O 14 NaCl + AgNO3 = AgCl ↓+ NaNO3 氮气 HNO3、NaNO2
【解析】(1)根据氧气约占空气体积的五分之一解答;根据硫在氧气燃烧产生蓝紫色火焰解答;(2)根据构成物质的微粒是不断运动的解答;根据能使石蕊溶液变为红色的物质显酸性,酸性物质中含有氢离子解答;(3)根据硫酸铁中的阳离子为铁离子解答;根据甲烷和氧气在点燃的条件下反应生成二氧化碳和氧气解答;(4) ①根据原子核外电子的排布规律及原子中质子数=电子数解答;②根据硝酸银与盐酸盐反应生成氯化银沉淀解答;③根据氮元素组成的单质为氮气解答;根据氮元素的化合价分析解答。(1)拉瓦锡通过实验测得,氧气约占空气体积的![]() ;硫在氧气燃烧会伴随明亮的蓝紫色火焰;(2)从微观视角看,“春雨丽润泽桃花开,微风拂面清香来”说明构成物质的微粒是不断运动的;CH3COOH、HCl等物质的水溶液都能使石蕊溶液变为红色的原因是:它们的溶波中都含有氢离子;(3) 硫酸铁中的阳离子为铁离子,离子符号为Fe3+;甲烷完全燃烧的化学方程式为CH4+2O2点燃2H2O+CO2;(4) ①根据原子核外电子的排布规律可知,第二层排8个,即x=8,又原子中质子数=电子数,即26=2+8+y+2,y=14;②硝酸银与盐酸盐反应生成氯化银,如NaCl+AgNO3=AgCl+NaNO3;③氮元素组成的单质为氮气,故图3中a处的1种物质名称氮气;NO2中氮元素的化合价为+4价,正确;HNO3中氮元素的化合价为+5价,错误;NH3H2O中氮元素的化合价为-3价,正确;NaNO2中氮元素的化合价为+3价,错误;NH4Cl中氮元素的化合价为-3价,正确。故其中位置放错的物质有HNO3、NaNO2。
;硫在氧气燃烧会伴随明亮的蓝紫色火焰;(2)从微观视角看,“春雨丽润泽桃花开,微风拂面清香来”说明构成物质的微粒是不断运动的;CH3COOH、HCl等物质的水溶液都能使石蕊溶液变为红色的原因是:它们的溶波中都含有氢离子;(3) 硫酸铁中的阳离子为铁离子,离子符号为Fe3+;甲烷完全燃烧的化学方程式为CH4+2O2点燃2H2O+CO2;(4) ①根据原子核外电子的排布规律可知,第二层排8个,即x=8,又原子中质子数=电子数,即26=2+8+y+2,y=14;②硝酸银与盐酸盐反应生成氯化银,如NaCl+AgNO3=AgCl+NaNO3;③氮元素组成的单质为氮气,故图3中a处的1种物质名称氮气;NO2中氮元素的化合价为+4价,正确;HNO3中氮元素的化合价为+5价,错误;NH3H2O中氮元素的化合价为-3价,正确;NaNO2中氮元素的化合价为+3价,错误;NH4Cl中氮元素的化合价为-3价,正确。故其中位置放错的物质有HNO3、NaNO2。


科目:初中化学 来源: 题型:
【题目】电导率是衡量电解质溶液导电能力大小的物理量.溶液电导率大小变化可以反映电解质溶液中离子浓度的大小变化。下图是向100mL一定溶质质量分数的Ba(OH)2溶液中分别滴加稀H2SO4溶液和稀Na2SO4溶液的过程中溶液电导率随时间变化图。回答下列问题。
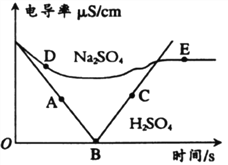
(1)写出Ba(OH)2与H2SO4反应的化学方程式_______________。
(2)若在图中A-E各点对应的溶液中滴加酚酞,则溶液呈红色的有____________。
(3) D-→E的反应过程中,溶液中数目始终增多的微粒有___________。
(4)经测定,B点时消耗稀H2SO4溶液50mL,且过滤后滤液质量为147. 67g。请计算原Ba(OH)2溶液的溶质质量分数__________(写出计算过程,各种稀溶液的密度都可看成1g·mL-1)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请同学们搭乘“化学地铁”一起畅游物质世界吧!如下图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。“2~5号站”各站的对应物质属于不同类别的纯净物。
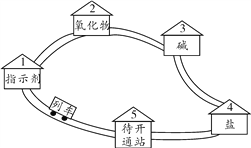
(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变__________色。
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠的化学方程式为____________________________。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为___(填一种)。
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为____________ (写一个)。
③“稀盐酸”列车途经“1、2、3号站”时,原“碳酸钠溶液”列车途经某站的对应物质必须更换为__________(写一种物质),“稀盐酸”列车方能走完。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答问题.

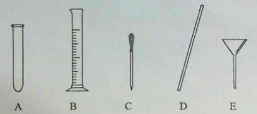
(1)仪器a的名称为 .
(2)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为 .用高锰酸钾制取氧气时,所选用的发生装置为 (填字母序号).
(3)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为 ;选用的收集装置是 (填字母序号),用此装置收集,检验气体是否收集满的操作是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室需配置一定浓度的硝酸钾溶液。
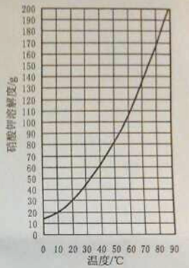
(1) 查阅硝酸钾溶解性。由右图可知,20℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配置40g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A、先移动游码到所需位置,再添加硝酸钾直到天平平衡
B、先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位1g/mL)
质量分数/% | 20 | 40 | 60 |
4 | 1.023 | 1.016 | 1.007 |
10 | 1.063 | 1.054 | 1.044 |
查看答案和解析>>
科目:初中化学 来源: 题型:
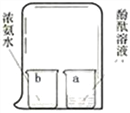
【题目】如图所示,在a烧杯中盛有酚酞溶液,在b烧杯中盛有浓氨水,有关现象和解释正确的是
选项 | 现象 | 解释 |
A | a烧杯溶液变红色 | b中氨气分子运动到a中,氨气溶于水,氨水呈碱性 |
B | a烧杯溶液变红色 | 氨气与酚酞反应生成红色物质 |
C | b烧杯溶液变红色 | b中氨气分子没有运动 |
D | b烧杯溶液变红色 | a中酚酞分子运动到b中,氨水呈中性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质王国举行一场趣味篮球赛。某队由五名“队员”组成:铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜。比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻,传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图。已知D位置上投篮的“队员”是个灭火“能手”。请回答:
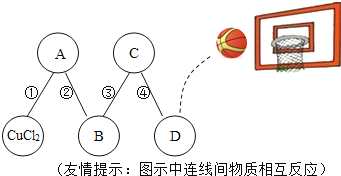
⑴D所代表物质的化学式是____________。
⑵图中反应②的化学方程式____________。图中反应④的化学方程式________________。
⑶图中反应③所属的基本反应类型是____________反应。
⑷为实现“快速进攻”,氯化铜除传球给A位置“队员”外,还能直接传球的另一名“队员”是________(填物质名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验是进行科学探究的重要方法,根据下图回答问题
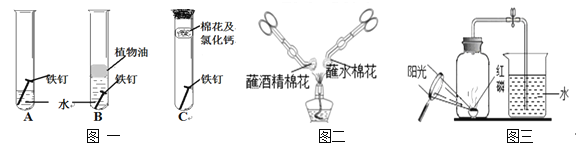
(1)图一为探究铁生锈的实验,B试管中植物油的作用是 __________________,证明铁生锈需要接触水的对比实验为___________(填字母)
(2)通过图二实验,可探究燃烧的条件之一是__________________ 该实验中两朵棉花都未能燃烧的主要原因是____________________
(3)图三为测定空气中氧气含量的改进装置,若实验结束后发现氧气含量比理论值偏小,则可能的原因是__________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~F六种物质共含H、C、O、N、Ca、Cu六种元素,分别为非金属单质、金属氧化物、非金属氧化物、酸、碱、盐中的一种。其中,A为温室气体,BC均为黑色固体,盐中不含金属。相邻物质之间能发生化学反应。
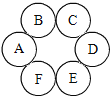
(1)A的固体俗称是_______________;
(2)E与F反应的现象是_________________________________;
(3)C与D反应的化学方程式____________________________________,属于________反应(填基本反应类型)。
(4)除相邻物质之间能发生化学反应外,还能相互反应的化学方程式____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com