
| A. | =7 | B. | >7 | C. | <7 | D. | 无法确定 |
分析 根据氢氧化钠、氢氧化钾与硫酸反应的化学方程式,判断改用20克氢氧化钾反应后剩余的是哪一种溶液,再根据当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;进行分析解答.
解答 解:氢氧化钠、氢氧化钾与硫酸反应的化学方程式分别是:
2NaOH+H2SO4═Na2SO4+2H2O
80 98
2KOH+H2SO4═K2SO4+2H2O
112 98
可知,80份质量的氢氧化钠与98份质量的硫酸恰好完全反应,而98份质量的硫酸能与112份质量的氢氧化钾恰好完全反应;中和一定质量的稀硫酸,需要M克NaOH,则改用M克KOH后,稀硫酸有剩余,溶液显酸性,反应后溶液的pH应当是小于7.
故选:C.
点评 本题难度不大,掌握中和反应应用,根据化学方程式的计算判断出反应后剩余的物质是正确解答本题的关键.


 阶梯计算系列答案
阶梯计算系列答案科目:初中化学 来源: 题型:实验探究题
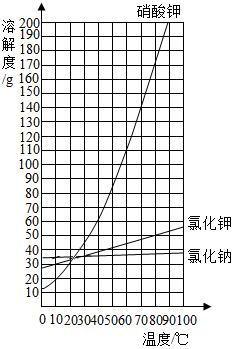 以下是某化学兴趣小组实施的从硝酸钾、氯化钠、氯化钾的混合物(其中氯化钠和氯化钾的质量和小于总质量的3%)中分离出硝酸钾的实验步骤:(三种物质的溶解度曲线见图)
以下是某化学兴趣小组实施的从硝酸钾、氯化钠、氯化钾的混合物(其中氯化钠和氯化钾的质量和小于总质量的3%)中分离出硝酸钾的实验步骤:(三种物质的溶解度曲线见图)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钠、氯化钙 | B. | 氯化钠、氯化镁 | ||
| C. | 氯化钠、碳酸镁 | D. | 尿素、硝酸钙、硝酸镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 组别编号 | 样品质量(克) | 加入稀硫酸质量(克) | 剩余固体质量(克) |
| 1 | 10 | 20 | 8.4 |
| 2 | 10 | 30 | 8 |
| 3 | 10 | 40 | 8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com