
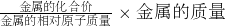 ,可计算一定量金属完全反应产生氢气的质量;
,可计算一定量金属完全反应产生氢气的质量; =0.2g;而不纯的镁样品与足量盐酸反应产生0.2g氢气,因此可判断样品镁中所含的两种金属与酸完全反应所产生氢气质量的平均值应与等质量镁产生氢气的质量相等;据此分析杂质的组成.
=0.2g;而不纯的镁样品与足量盐酸反应产生0.2g氢气,因此可判断样品镁中所含的两种金属与酸完全反应所产生氢气质量的平均值应与等质量镁产生氢气的质量相等;据此分析杂质的组成. =0.2g;所以样品镁中所含的两种金属与酸完全反应所产生氢气质量的平均值应与等质量镁产生氢气的质量相等;
=0.2g;所以样品镁中所含的两种金属与酸完全反应所产生氢气质量的平均值应与等质量镁产生氢气的质量相等; ≈0.09g<0.2g;所以,若样品中含有铁则同时还须含有等质量金属完全反应产生氢气质量大于0.2g的金属;
≈0.09g<0.2g;所以,若样品中含有铁则同时还须含有等质量金属完全反应产生氢气质量大于0.2g的金属; ≈0.27g>0.2g;所以,若样品中含有铝则同时还须含有等质量金属完全反应产生氢气质量小于0.2g的金属;
≈0.27g>0.2g;所以,若样品中含有铝则同时还须含有等质量金属完全反应产生氢气质量小于0.2g的金属; ≈0.07g<0.2g;所以,若样品中含有锌则同时还须含有等质量金属完全反应产生氢气质量大于0.2g的金属;
≈0.07g<0.2g;所以,若样品中含有锌则同时还须含有等质量金属完全反应产生氢气质量大于0.2g的金属;

科目:初中化学 来源: 题型:

| 反应前 | 充分反应后 | |
| 硬质玻璃管③+样品的质量 | Ml | M2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:
某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:查看答案和解析>>
科目:初中化学 来源:江苏省泰兴市实验中学2012届九年级12月阶段测试化学试题 题型:058
某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体).实验过程是:
①取一段镁带样品,准确称得其质量为0.030 g.
②往量气管内装水至低于刻度“0”的位置,按图中所示(未装药品)装配好仪器.

③检查装置气密性.
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞.
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置.
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应.
⑦待冷却至室温后,再次记录量气管中液面位置.
⑧算出量气管中增加的气体体积为23.96 mL.
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和.
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式:________.
(2)能否用托盘天平称量0.030 g镁带样品________.(填“能”或“不能”)
(3)若不改变温度,如何检查图中所示装置的气密性?________.
(4)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果________(填“是”或“否”).理由是________.
(5)若实际测得氢气的体积与理论值相比偏大,则可能的原因是________.
(6)经换算,该实验获得的氢气质量为0.002 g.求:0.030 g该不纯镁带中单质镁的质量分数(通过计算回答)?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com