
| A. | 硫酸亚铁 | B. | 盐酸 | C. | 氢氧化钠 | D. | 硫酸铜 |
分析 根据金属活动性顺序,验证金属的活动性顺序的试剂是否合理,可根据“反应则活泼,不反应则不活泼”进行分析判断,通过分析提供的试剂所能得到的结论,确定是否能得出铝和铜两种金属的活动性顺序.
解答 解:A、锌与硫酸亚铁能反应,铜与硫酸亚铁不反应,能用来比较锌与铜两种金属活动性的强弱
B、锌与盐酸反应,铜与盐酸不反应,能用来比较锌与铜两种金属活动性的强弱
C、锌、铜与氢氧化钠溶液都不反应,不能用来比较锌与铜两种金属活动性的强弱.
D、锌与硫酸铜溶液反应置换出铜,说明了活动性锌>铜,能用来比较锌与铜两种金属活动性的强弱.
故选C.
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:选择题
| A. | 清澈的温泉水是混合物 | |
| B. | 活性炭可用于净化温泉水的味道 | |
| C. | 检验温泉水是硬水还是软水可用肥皂水 | |
| D. | 过滤可以除去温泉水中的可溶性杂质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
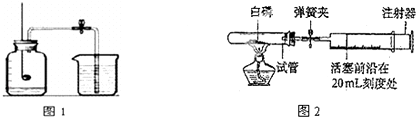
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它是由氧化铜、水和二氧化碳组成 | |
| B. | 它一定含有C、H、Cu元素,不含有O元素 | |
| C. | 它一定含有C、Cu元素,可能含有H、O元素 | |
| D. | 它由C、H、O、Cu四种元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是实验室制取二氧化碳的装置,据图回答下列问题:
如图是实验室制取二氧化碳的装置,据图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
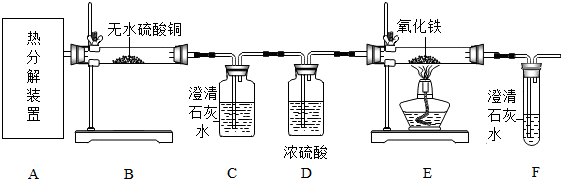
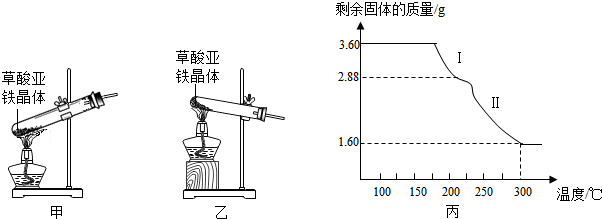
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com