

分析 饱和溶液的质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液中溶质和溶剂的质量比;
溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%.
解答 解:(1)40℃时,甲的溶解度大于乙的溶解度,因此饱和溶液中溶质的质量分数关系是甲>乙;
20℃时,将50g乙物质放入100g水中,升温至40℃,只能够溶解40g,因此溶液中溶质和溶剂的质量比为:40g:100g=2:5;
(2)①上述实验过程中属于不饱和溶液的是A、C;
②溶质的质量分数相同的是B、C、E.
故填:>乙;2:5;A、C;B、C、E.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:初中化学 来源: 题型:选择题
| A. | 10mL酒精和10mL水混合后体积小于20mL,是因为分子变小了 | |
| B. | NH4NO3不能与熟石灰同时施用 | |
| C. | 富硒大米、低钠盐中的“硒”和“钠”指的是原子 | |
| D. | 中学生每天喝的牛奶是一种溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 回收利用废旧金属是保护金属资源的有效途径之一 | |
| B. | 人呼出的气体主要成分为二氧化碳,不能用排水法收集 | |
| C. | 自然界的水经过沉淀、过滤、吸附等净化处理后,水的硬度并没有明显降低 | |
| D. | 天然气的主要成分为甲烷 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
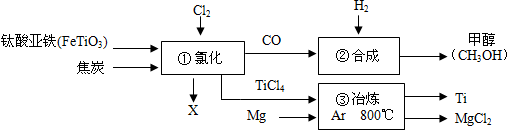
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
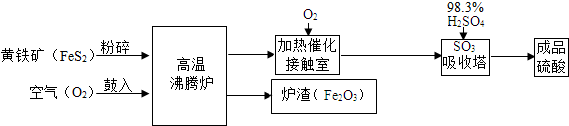
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
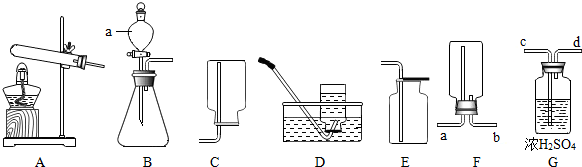
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com