
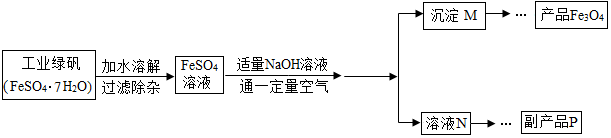
分析 (1)根据常见的铁的氧化物来分析;
(2)根据氢氧化钠与硫酸亚铁反应的生成物来判断副产品,根据冷却热饱和溶液的过程考虑操作顺序;
(3)如果氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了,根据方程式计算出Fe(OH)2和Fe(OH)3的相对分子质量比,别忘了前面的系数.
解答 解:(1)常见的铁的氧化物还有氧化铁和氧化亚铁,在氧化铁中,铁显+3价,氧化亚铁中铁显+2价,氧元素均为-2价,故填:Fe2O3;FeO;
(2)氢氧化钠与硫酸亚铁反应的生成物是氢氧化亚铁与硫酸钠,因为氢氧化亚铁属于另一反应的反应物了所以副产品是硫酸钠;冷却热饱和溶液 的过程是先加热,再降温,析出晶体后过滤再通过加热除去结晶水即可;
(3)通过反应Fe(OH)2+2Fe(OH)3?Fe3O4+4H2O可知,Fe(OH)2和Fe(OH)3都是反应物,如果不控制“一定量空气”氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了;由化学方程式Fe(OH)2+2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2O可知,Fe(OH)2和Fe(OH)3的最佳质量比为:$\frac{90}{2×107}$=$\frac{45}{107}$.
故答案为:(1)Fe2O3;FeO;(2)硫酸钠,c,a;(3)防止氢氧化亚铁全部被氧化为氢氧化铁;45:107.
点评 通过回答本题知道了制取四氧化三铁的方法,溶解需要的仪器,由溶液析出晶体的方法.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
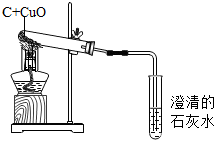 如图所示是木炭还原氧化铜的实验,写出该反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 ↑.实验完毕后,发现试管内仍有黑色固体物质存在,其中网罩的作用是提高温度.澄清石灰水的作用是验证反应是否产生二氧化碳.
如图所示是木炭还原氧化铜的实验,写出该反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2 ↑.实验完毕后,发现试管内仍有黑色固体物质存在,其中网罩的作用是提高温度.澄清石灰水的作用是验证反应是否产生二氧化碳.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
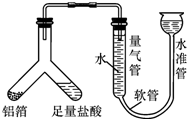 梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.
梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上表明锡纸的材质为“铝箔”.| 实验一:4mL8%CuSO4溶液 | 实验二:4mL8%CuCl2溶液 | |
| 实验 现象 | 短时间内无变化,一段时间后铝片上才出现少量红色的铜 | 铝片上迅速有红色的铜出现 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
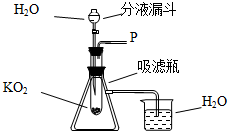 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.首先他将少量超氧化钾(KO2)粉末用脱脂棉包裹,没有任何变化(已知脱脂棉与超氧化钾不反应),然后向包有超氧化钾(KO2)粉末的脱脂棉上滴加少量的水,则脱脂棉迅速发生剧烈的燃烧(比在空气中燃烧还剧烈).小冬对此很感兴趣,于是,他和同学们进行探究.请你也参与他们的本次探究活动.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.首先他将少量超氧化钾(KO2)粉末用脱脂棉包裹,没有任何变化(已知脱脂棉与超氧化钾不反应),然后向包有超氧化钾(KO2)粉末的脱脂棉上滴加少量的水,则脱脂棉迅速发生剧烈的燃烧(比在空气中燃烧还剧烈).小冬对此很感兴趣,于是,他和同学们进行探究.请你也参与他们的本次探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 需区分的物质 | 方法一 | 方法二 |
| A | 氮气和二氧化碳 | 分别通入澄清石灰水 | 分别通入石蕊溶液 |
| B | 碳酸钠溶液与硫酸钠溶液 | 加硝酸钡溶液 | 加稀盐酸 |
| C | 碳酸氢铵与硫酸钾 | 取样品闻气味 | 观察颜色 |
| D | 棉布与涤纶布 | 取样品点燃闻气味 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
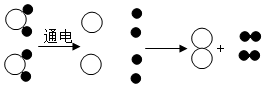 如图是电解水中,分子分解过程示意图.你能得出的规律和结论.
如图是电解水中,分子分解过程示意图.你能得出的规律和结论.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com