
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2气体(CO) | 过量的氧气 | 点燃 |
| B | Fe2O3(Fe) | 足量的盐酸 | 过滤 |
| C | FeSO4溶液(CuSO4) | 足量的锌 | 过滤 |
| D | O2(H2O) | 浓硫酸 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项所采取的方法错误.
B、Fe和Fe2O3均能与足量的盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、FeSO4溶液和CuSO4均能与足量的锌反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、浓硫酸具有吸水性,且不与氧气反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:初中化学 来源: 题型:解答题
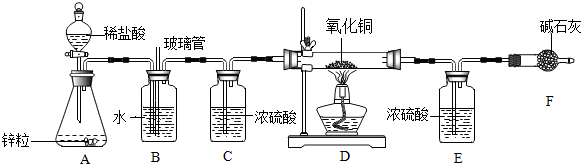
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
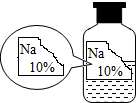 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.
实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下稀溶液的pH | 7 | 13 | 11 | 9 |
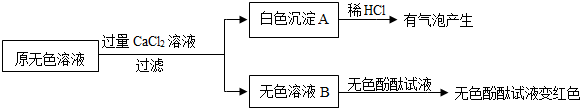
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
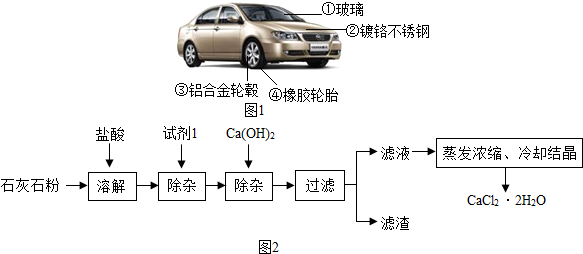
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
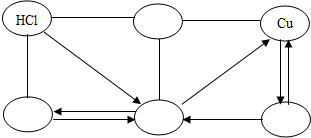 如图所示是六种物质间的反应及转化关系.用“-”表示两种物质能发生化学反应,用“→”表示一种物质可以通过一步反应转化为另一种物质.A、B、C含有相同的金属元素,且分别属于不同类别的化合物,且A为黑色固体,C为蓝色固体,D为一种无色盐溶液.
如图所示是六种物质间的反应及转化关系.用“-”表示两种物质能发生化学反应,用“→”表示一种物质可以通过一步反应转化为另一种物质.A、B、C含有相同的金属元素,且分别属于不同类别的化合物,且A为黑色固体,C为蓝色固体,D为一种无色盐溶液.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com