


科目:初中化学 来源: 题型:
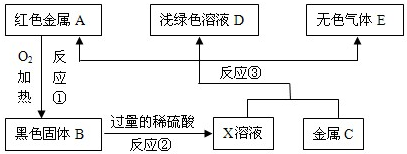
 已知A、B、C、D、E是初中化学常见的五种物质,其中A、D是黑色固体,A为黑色固体单质,D为黑色固体氧化物,且其中含有人类使用最广泛的金属元素,B、C、E是无色气体,.它们在一定条件下的转化关系如下图所示(其他反应物和生成物已略去).
已知A、B、C、D、E是初中化学常见的五种物质,其中A、D是黑色固体,A为黑色固体单质,D为黑色固体氧化物,且其中含有人类使用最广泛的金属元素,B、C、E是无色气体,.它们在一定条件下的转化关系如下图所示(其他反应物和生成物已略去).查看答案和解析>>
科目:初中化学 来源: 题型:
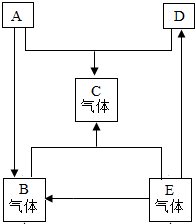
 23、已知A、B、C、D、E是初中化学里常见的五种物质,它们在一定条件下能发生如图所示的转化,其中反应①是复分解反应,E是造成温室效应的主要气体.
23、已知A、B、C、D、E是初中化学里常见的五种物质,它们在一定条件下能发生如图所示的转化,其中反应①是复分解反应,E是造成温室效应的主要气体.查看答案和解析>>
科目:初中化学 来源: 题型:
 A、B、C、D、E是常见物质,其中B和E是空气中两种气体,C是铁锈主要成分.如图所示,直线表示相互间能够反应,箭头表示转化的方向.
A、B、C、D、E是常见物质,其中B和E是空气中两种气体,C是铁锈主要成分.如图所示,直线表示相互间能够反应,箭头表示转化的方向.查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?徐州二模)A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质;C是红棕色固体;E是水溶液可使酚酞试液变为红色的盐.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
(2013?徐州二模)A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质;C是红棕色固体;E是水溶液可使酚酞试液变为红色的盐.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 A、B、C、D、E是初中化学中常见的5种物质,它们都含有一种相同的元素,如图表示各物质之间的转化关系.其中,A为食盐的主要成分,B中含钡元素,D、E的溶液都有颜色,
A、B、C、D、E是初中化学中常见的5种物质,它们都含有一种相同的元素,如图表示各物质之间的转化关系.其中,A为食盐的主要成分,B中含钡元素,D、E的溶液都有颜色,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com