
下列说法正确的是( )
A.HIO与HCN均为含有极性键的直线形极性分子
B.SiO2与C02均为每摩含有4×6.02×1023对共用电子对的酸性氧化物
C.Na2S浓溶液与稀盐酸分别滴加到饱和AgCl溶液中均一定有沉淀产生
D.明矾与离子交换树脂均能将海水进行淡化
【考点】判断简单分子或离子的构型;酸、碱、盐、氧化物的概念及其相互联系;难溶电解质的溶解平衡及沉淀转化的本质.
【分析】A、HIO中心原子O电子对数为2+ =4,杂化方式为SP3,分子构型为V型;
=4,杂化方式为SP3,分子构型为V型;
B、SiO2与C02每一摩尔Si和C均含有4mol共价键;
C、稀盐酸中氯离子浓度若小于饱和AgCl溶液中氯离子浓度,则不会产生沉淀;
D、海水淡化是使海水中盐分减少,即减少钠离子和氯离子的量.
【解答】解:A、HIO中心原子O电子对数为2+ =4,杂化方式为SP3,分子构型为V型,故A错误;
=4,杂化方式为SP3,分子构型为V型,故A错误;
B、SiO2与C02每一摩尔Si和C均含有4mol共价键,则每摩含有4×6.02×1023对共用电子对,SiO2与C02均属于酸性氧化物,故B正确;
C、稀盐酸中氯离子浓度若小于饱和AgCl溶液中氯离子浓度,相当于稀释了饱和AgCl溶液,所以不会产生沉淀,故C错误;
D、明矾水解生成絮状沉淀可以吸附水中漂浮物,不能吸附阴阳离子,故不能淡化海水,故D错误.
故选:B.
【点评】本题考查了分子构型和极性、化学键数目的简单计算、难溶电解质的溶解平衡和沉淀转化的本质,综合性强,难度中等.


科目:初中化学 来源: 题型:
为除去下列物质中的杂质(括号内为杂质),下列操作方法能达到目的的是
| 选项 | 物质(杂质) |
|
| A | CO2(H2O) | 将气体通过盛有火碱的干燥管 |
| B | Cu(CuO) | 通入足量氧气并加热 |
| C | Na2SO4(Na2CO3) | 加盐酸至恰好不再产生气泡为止 |
| D | FeCl2(CuCl2) | 加入足量铁屑,充分反应后过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:
用化学用语填空:
①2个镁原子 ▲ ;②铁离子 ▲ ;③水中氧元素显-2价 ▲ ;④铵根离子 ▲ ;
⑤2个碳酸分子 ▲ ;⑥光合作用得到的单质是 ▲ ;⑦地壳中最多的金属元素 ▲ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
 右图是某硝酸铵产品包装袋上的标签说明。仔细分析标签说明,然后回答下列有关问题。
右图是某硝酸铵产品包装袋上的标签说明。仔细分析标签说明,然后回答下列有关问题。
(1)硝酸铵由 ▲ 种元素组成。
(2)硝酸铵的相对分子质量是 ▲ 。
(3)硝酸铵中N、H、O的质量比是 ▲ 。
(4)该硝酸铵产品中所含硝酸铵的质量分数是 ▲ 。
(5)某农民有10亩地,开始准备每亩地需施用66kg纯硫酸铵[(NH4)2SO4]来促进农作物生长,现因纯硫酸铵缺货,改施用上述硝酸铵产品,若要使两种化肥达到相同的肥效(即氮元素的质量相同),则该农民总共需购买多少kg上述硝酸铵产品?(写出计算过程)(2分)
▲
查看答案和解析>>
科目:初中化学 来源: 题型:
氢溴酸、硫酸钡是用途广泛的工业产品.实验室利用SO2、Br2模拟工业上精制氢溴酸同时得副产品硫酸钡,有关流程如下:
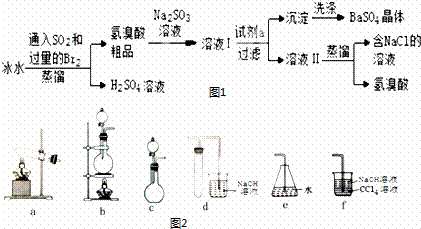
(1)实验室制Br2的反应原理为2NaBr+3H2SO4(浓)+MnO2 2NaHSO4+MnSO4+Br2↑+2H2O 则下列装置中,可用来制取Br2的是 (填字母,下同),可用来吸收SO2尾气的是 .
2NaHSO4+MnSO4+Br2↑+2H2O 则下列装置中,可用来制取Br2的是 (填字母,下同),可用来吸收SO2尾气的是 .
(2)试剂a为 ,使用冰水的目的是 .
(3)加入Na2SO3的目的是除去 ,所加Na2SO3的量的多少是否会影响氢溴酸的产量? (填“影响”或“不影响”).
(4)为得到纯净的BaSO4晶体,洗涤沉淀的具体操作为: .
(5)工业上氢溴酸常显淡黄色,可能的原因是:①含有杂质Fe3+②含有杂质Br2 ③含有杂质Fe3+、Br2,只用下列一种试剂就能分析产生淡黄色的原因,该试剂是 (填字母).
a.KMnO4 b.CCl4 c.NaOH d.KSCN.
查看答案和解析>>
科目:初中化学 来源: 题型:
下面是初中化学中常见的四个基本实验。请回答下列问题。




A B C D
(1)图A实验可以得出有关氧气含量的结论是 ,
如果测得的结果偏低,可能的原因之一是 。
(2)图B实验中酒精灯加网罩的作用 。
(3)图C实验中铜片两侧分别放有同样大小的乒乓球碎片和滤纸碎片,观察到乒乓球
碎片先燃烧,由此可以得出燃烧的条件之一 。
(4)图D实验中玻璃管中的现象是 ,
,
反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com