
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCI | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
分析 Ⅰ.由KNO3、NaCl在不同温度下的溶解度表,比较出两种物质在40℃时的溶解度即可;结合饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}$×100%,进行分析解答.
Ⅱ.大多数物质的溶解度随着温度的升高而增大,多数物质的不饱和溶液变为饱和溶液,常用的方法有:增加溶质、蒸发溶剂、降低温度,据此进行分析解答.
Ⅲ.根据20℃时,氯化钠的溶解度为36.0g,进行分析解答.
Ⅳ.根据氯化钠的溶解度受温度的影响变化不大,进行分析解答.
解答 解:Ⅰ.由KNO3、NaCl在不同温度下的溶解度表,两种物质在40℃时硝酸钾的溶解度较大;该温度时KNO3饱和溶液的质量分数为$\frac{63.9g}{63.9g+100g}$×100%.
Ⅱ.硝酸钾的溶解度随着温度的升高而增大,将KNO3的不饱和溶液转化为饱和溶液,可采用加入硝酸钾、蒸发溶剂、降低温度等方法.
Ⅲ.20℃时,氯化钠的溶解度为36.0g,其涵义是20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态,则20℃时,将20gNaCl放入50g水中,最多只能溶解18g,所得溶液的质量是18g+50g=68g.
Ⅳ.氯化钠的溶解度受温度的影响变化不大,从NaCl溶液中得到NaCl晶体的方法是蒸发结晶.
故答案为:Ⅰ.硝酸钾;$\frac{63.9g}{63.9g+100g}$×100%;Ⅱ.加入硝酸钾等;Ⅲ.68;Ⅳ.蒸发结晶.
点评 本题难度不大,掌握常见物质的溶解度受温度影响的变化趋势、不饱和溶液变为饱和溶液的方法、结晶的方法等是正确解答本题的关键.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:解答题
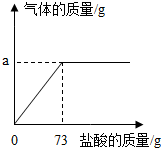 为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应)
为了分析生铁中铁的含量,某学习小组进行了实验研究:取6g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见图).(说明:生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 18g | B. | 44g | C. | 48g | D. | 62g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 因为H2O和H2O2的组成元素相同,所以它们的化学性质相同 | |
| B. | 因为酚酞试液遇碱变红色,所以能使酚酞变红色的一定是碱 | |
| C. | 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成中一定含有C、H和O | |
| D. | 有化合价升降的反应是氧化还原反应,所以复分解反应一定不是氧化还原反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
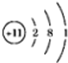 钠及其化合物是中学化学学习和研究的重要内容.
钠及其化合物是中学化学学习和研究的重要内容.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 如图所示,A~I为初中化学中常见的物质,已知A为石灰石 D为蓝色沉淀,C和E为只含一种物质的溶液,I为生命之源.“→”表示物质间存在着相互转化的关系(部分生成物未标出).回答下列问题:
如图所示,A~I为初中化学中常见的物质,已知A为石灰石 D为蓝色沉淀,C和E为只含一种物质的溶液,I为生命之源.“→”表示物质间存在着相互转化的关系(部分生成物未标出).回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
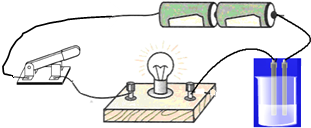 如图是验证溶液能否导电的装置,烧杯中的溶液为氢氧化钙饱和溶液.
如图是验证溶液能否导电的装置,烧杯中的溶液为氢氧化钙饱和溶液.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 两个氯原子Cl2 | B. | 氦气中氦元素的化合价为零$\stackrel{O}{{N}_{2}}$ | ||
| C. | 氧化镁:MgO2 | D. | 二个氢氧根离子2OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com