
�⻯�ƣ�CaH2�������ǵ�ɽ��Ա���õ���Դ�ṩ����ij��ѧ��ȤС��������ͼ1��ʾ��װ���Ʊ��⻯�ƣ��䷴Ӧ�Ļ�ѧ����ʽΪ��Ca+H2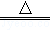 CaH2��
CaH2��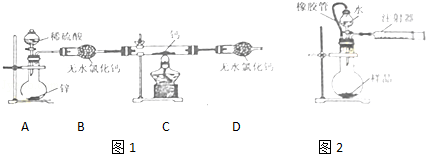
��1��CaH2�иƺ���Ԫ�صĻ��ϼ۷ֱ�Ϊ�� ����װ���е���ˮ�Ȼ��Ƹ���װ��Ҳ������ �������森
��2�����ø�װ�ý���ʵ�飬�������£����װ�õ������Ժ�װ��ҩƷ����Һ©���������� �����밴��ȷ��˳���������в������ţ���
�ټ��ȷ�Ӧһ��ʱ�� ���ռ����岢�����䴿�� �۹رշ�Һ©������ ��ֹͣ���ȣ������ȴ
��3��Ϊ��ȷ�Ͻ���װ��C�������Ѿ����Ӧ��B��C֮��������һװ��X��װ��X�м�����Լ����� ����������δ��ָ��װ��X�е�����Ϊ�� ����
��4��Ϊ�˲�������ʵ�����Ƶõ��⻯�ƵĴ��ȣ���С���ȡmg���Ƶ���Ʒ������ͼ2��ʾװ�ý��вⶨ��������Һ©����������Ӧ����������ȴ��ע���������ɷ�Ӧǰ��V1mL�̶ȴ��仯��V2mL�̶ȴ���V2��V1�������ܶ�Ϊdg/mL��
���ܵ�����Ϊ��a���� ����b���� ����
��������Һ©������������CaH2+H2O�TCa��OH��2+H2���ķ�Ӧ�⣬�����п��ܷ����ķ�ӦΪ�� ����
����w��ʾ�⻯�ƵĴ��ȣ�����һ����ʽ��ʾ��d��V1��V2��w֮��Ĺ�ϵ���� ��
�ܸ�С����ͬѧ��Ϊȥ�����ӵ�ע������ҲҪ������⻯�ƵĴ��ȣ���ͬ����ȡmg��Ʒ��������ƿ�к��ȡ��Ӧǰ������Ϊm1g����Ӧ�������Ϊm2g����ͬѧ��ʾ����m��m1��m2��w֮��Ĺ�ϵ�ĵ�ʽΪ�� ��
��1��+2����1����ʯ�ң���2���ڢ٢ܢۣ���3����ˮ����ͭ�������������4����a��ƽ���Һ©������ƿ�е���ѹ��b������ˮ���£���Ca+2H2O�TCa��OH��2+H2������ +
+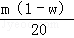 =��V2��V1����d����
=��V2��V1����d���� +
+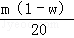 =m1��m2��
=m1��m2��
���������������1����CaH2�иƺ���Ԫ�صĻ��ϼ۷ֱ�Ϊ+2����1�����ڼ�ʯ������ˮ�ԣ�װ���е���ˮ�Ȼ��Ƹ���װ��Ҳ���ü�ʯ�������棻
��2������������һ�ֿ�ȼ�Ե�����������Ļ�������ڵ�ȼʱ����Ҫ��ը�����ԣ�ʵ��ʱ��Ӧ��Һ©��������ʹ�⻯����ˮ��Ӧ�����������ռ������������䴿�ȣ���ͨ��һ����ž�װ���еĿ��������ȷ�Ӧһ��ʱ�䣬�ȷ�Ӧ��ɺ�ֹͣ���ȣ������ȴ����رշ�Һ©�����������ԣ���ȷ��˳���ǣ��ڢ٢ܢۣ�
��3��������ˮ����ͭ����ˮ�������ɫ������ͭ���壮���ԣ�Ϊ��ȷ�Ͻ���װ��C�������Ѿ����Ӧ��B��C֮��������һװ��X��װ��X�м�����Լ�����ˮ����ͭ��������δ��ָ��װ��X�е�����Ϊ�������ɫ��
��4�����������ܽ���Һ©�����ձ���ͨ�������������ǣ�a��ƽ���Һ©������ƿ�е���ѹ��b������ˮ���£�
�����ڸ��ǽϻ��õĽ�������ˮ��Ӧ�����ԣ����ܷ����ķ�Ӧ�У�Ca+2H2O�TCa��OH��2+H2����
����������������V2mL��V1mL����dg/mL=��V2��V1����dg
���⻯����ˮ��Ӧ���ɵ�����������Ϊx
CaH2+H2O�TCa��OH��2+H2��
42 2
mg��w x ��ã�x=
��ã�x= g
g
�����ˮ��Ӧ���ɵ�����������Ϊy
Ca+2H2O�TCa��OH��2+H2����
40 2
mg��1��w�� y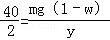 ��ã�y=
��ã�y=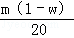 g
g
���ԣ� g+
g+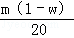 g�T��V2��V1����dg
g�T��V2��V1����dg  +
+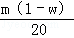 =��V2��V1����d
=��V2��V1����d
���������غ㶨�ɿ�֪����������������Ϊ��m1g��m2g
�����������֪�� g+
g+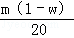 g=m1g��m2g
g=m1g��m2g
���ԣ� +
+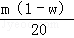 =m1��m2
=m1��m2
���㣺���ʵ��ת�����Ʊ�������ľ��������ӣ�����������ȡ�ͼ��飻����Ũ������ռ������ȷ�����ܸ�������壻�й�Ԫ�ػ��ϼ۵ļ��㣮
�����������ǽ�ʵ��ͼ�������һ���ۺ����ͣ��ڼ�����Ҫע�⣬����������һ���������⻯����ˮ��Ӧ���ɵģ���һ�������Ը���ˮ��Ӧ��Ӧ���ɵģ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
���������1С�⣬��12�֣�
27.��11�֣������ƣ�Na2S4�������������ײⶨ�����������������������Ӧԭ��Ϊ��2 Na2S4 + O2 + 2H2O =" 8S��+" 4 NaOH��
��ʵ�����ϡ�
�������ƣ�Na2S4������Է�������Ϊ ��������Ԫ�ص���������Ϊ �������ȷ��0.1%����
������������ʱ����������е�ˮ������Ӧ�����������ж��������⡣
��NaOH��Һ�ʼ��ԣ����������⡢������̼�������������������
����������ƣ�Na2S2O3��������ˮ����������NaOH��Һ����Ӧ��
��ʵ����̡�
��ȡ̼���ơ� ��ۻ�Ϻ������Թ��У����ȣ���ͼ1��ʾ���г�װ������ȥ�����Ƶ�Na2S4����ӦΪ4Na2CO3 + 12S + X  2 Na2S4+ 2 Na2S2O3 + 4CO2��X �Ļ�ѧʽΪ ��պ��ŨNaOH ��Һ������������ ��
2 Na2S4+ 2 Na2S2O3 + 4CO2��X �Ļ�ѧʽΪ ��պ��ŨNaOH ��Һ������������ �� 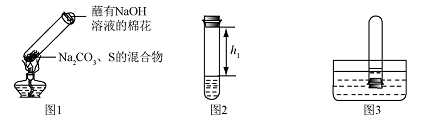
����ȴ��ȡ����������һ��ʱ�䣬������Թ��м���10mlˮ��Ѹ���������������������Һ�����������صľ��룬��¼����h1����ͼ2��ʾ��
�۽����Թܲ���ˮ�У���ͼ3����ȡ���������۲쵽
���������������Թ�ȡ����������������Һ�����������صľ��룬��¼����h2��������h1:h2��
�ܰ��բ١������ظ�ʵ��2�Σ�3��ʵ���������±���ʾ��
| | ��1�� | ��2�� | ��3�� |
| h1/cm | 11.2 | 11.4 | 11.6 |
| h2/cm | 8.9 | 9.1 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
����һ����������������ɳ�Ȳ��������ʺ�����Na2SO4��MgCl2��CaCl2�ȿ��������ʵĴ�����Ʒ��ijʵ��С�����û�ѧʵ���ҳ��������Դ�����Ʒ�����ᴿ���ᴿ�������£�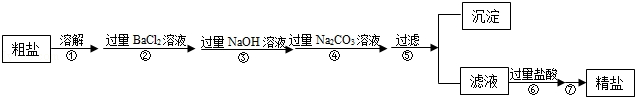
������ᴿ����ش��������⣮
��1������ߵIJ�������Ϊ ��
��2����д��ʵ�鲽��������漰�Ļ�ѧ����ʽ ��
��3��������м�����������Ŀ���� ��
��4������ںͲ���� ������ԡ������ԡ����ߵ��������� ��
��5�����鲽�����Na2CO3��Һ�ѹ����ķ����� ��
��6���ӵ�ʳ�������Ϣ��ͼ��ʾ��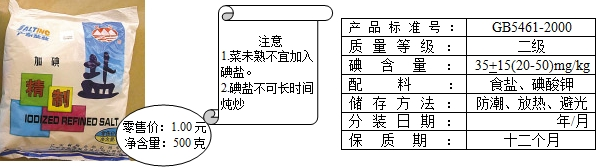
ʳ���еĵ���أ�KIO3�������������£����Խ��⻯�أ�KI����ɵ⣨I2������ѧ����ʽ���£�
KIO3+5KI+6HCl=6KCI+3I2+3H2O
����װ�е⻯�غ͵��ۻ��Һ���Թ��У�����ϡ���Ὣ��Һ�ữ���ټ���ʳ�Σ���ʳ�����е⻯�أ������ʳ�κ��ʵ������ ��
��Сǿͬѧ���ⶨ�ӵ����е�Ԫ�ص�����������ʵ�鲽�����£�ȡ10gʳ����Ʒ���Թ��м�ˮ�ܽ⣬�������KI�ĺ͵��ۻ����Һ���ٵ���ϡ���Ὣ��Һ�ữʹ���ַ�Ӧ������Һ�����ԣ������Թ��еμ������������Һ��Na2S2O3����������ѧ��Ӧ����ʽΪ��2Na2S2O3+I2�TNa2S4O6+2NaI
��������������Ϊ0.237%Na2S2O3��Һ2gʱ��I2ǡ�÷�Ӧ��ȫ��ͨ�������жϸ�ʳ����Ʒ�Ƿ�ϸ���֪Na2S2O3����Է�������Ϊ158����д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
ij��ȤС��Ϊ�ⶨʵ������һƿ���õĹ���������Һ�����ʵ�����������ʵ���������������ͼ��ʾ��
��1��ʣ��Ļ�����ж������̵�����Ϊ ��g����Ӧ��������������Ϊ�� ��g��
��2������ù���������Һ������������������������������0.1%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�ڹ�ҵ���ô����ʯ��ʯΪԭ���Ʊ��ռ��Ҫ������ͼ��ʾ��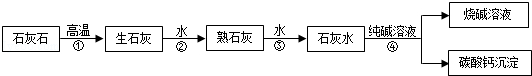
��1���ڢ٩����ĸ������У������˷ֽⷴӦ���� ������ţ���
��2�������ռ���Һ�к�������Na2CO3�ľ��巽���� ��
��3���������£���53g��������Ϊ10%��Na2CO3��Һ��3000g����ʯ��ˮ��ֻ�ϣ�ǡ����ȫ��Ӧ������ʱ����NaOH��Һ�������Ƕ��٣�����������ȷ��0.1g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
ij��ѧ��ȤС��Ϊ�˲ⶨһ������ˮ������ĺ�����ȡ100g��ˮ���ձ��У�����120g��������Ϊ10%������������Һ��ǡ����ȫ��Ӧ����ˮ������������ɷֲ����������Ʒ�Ӧ��������㣺��ˮ�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
ͨ�����ˮ�Ƶõ����������ڵ��ӹ�ҵ���Ʊ��ߴ��ȹ裮��Ҫ�Ƶ�0.4kg����������������ˮ�������Ƕ��٣���д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
С����Э����ʦ����ʵ����ʱ��������һƿ̼���ƺ��Ȼ�����ɵĻ��Һ������ⶨ����Һ��̼���ƺ��Ȼ��Ƶ�����������Ϊ����Ʋ�����������ʵ�顣
��ʵ��1��ȡ�û��Һ50 g ����������μ���ϡ���ᣬ������ϡ���������Ϊ20 g��40 g��60 g ʱ������������������±���������ܽ�Ⱥ��Բ��ƣ���
��ʵ��2����ȡ����Һ50 g ������һ����ϡ�����ַ�Ӧ�����Һ��pH=7��Ȼ���ټ�����������Һ�����ʵ�����ݼ���ͼ��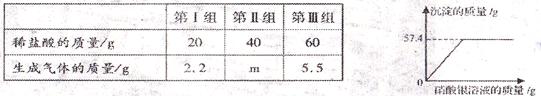
�Է������㣺
��1����ʵ��1���У��ڶ������� m Ϊ g��
��2�����Һ��̼���Ƶ����������Ƕ��٣�
��3�����Һ���Ȼ��Ƶ����������Ƕ��٣�����������ȷ��0.1%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����ͼ��Ϊ���װ�õ������ԣ�����װ�����¶Ȳ��䣬�����ܵ�ĩ������װ��ˮ���ձ��С���װ�õ����������ã��ձ��ڵ��ܴ�������Ȧ���֣���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com