
分析 物理性质是指物质不需要发生化学变化就表现出来的性质.化学性质是指物质在化学变化中表现出来的性质.而化学变化的本质特征是变化中有新物质生成,因此,判断物理性质还是化学性质的关键就是看表现物质的性质时是否有新物质产生.可以据此完成(1)和(2)两小题.
(3)根据该气体的物理性质考虑;
(4)根据硫化氢有毒,能溶于水进行分析;
(5)根据实验室制取硫化氢的反应物是固体和液体,反应条件是常温,硫化氢密度比空气大,过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
(6)根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
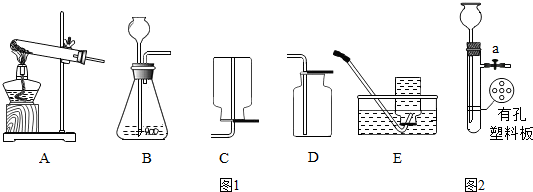
(7)根据图2装置可以通过压强的改变,控制反应的发生和停止进行分析;
(8)根据分液漏斗可以控制液体的滴加速度进行分析.
解答 解:(1)低洼地的人畜死亡率高,说明该气体密度比空气大,头埋在和着烂死的潮湿的草里,却幸免于中毒,说明该气体易溶于水;
(2)高压天然气携带一种有毒气体从地下喷出,所以该气体有毒;点燃了喷出的气体,说明该气体具有可燃性;
(3)因为该气体易溶于水,所以要用湿毛巾捂住口鼻,又因为该气体密度比空气大,所以要向高处跑;
(4)当地政府已经通知下游群众不要饮用河沟水,因为硫化氢能溶于水,有毒;
(5)实验室制取硫化氢的反应物是固体和液体,反应条件是常温,硫化氢密度比空气大,所以发生装置是B,收集装置是D,此装置还可用来制取氧气,过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(6)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以发生装置选A,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,要收集到较纯净的氧气应选用E;
(7)图2装置可以通过压强的改变,控制反应的发生和停止,所以改进后该装置的优点是可控制反应随时发生和停止;
(8)分液漏斗可以控制液体的滴加速度.
故答案为:(1)无色有臭鸡蛋气味的气体,能溶或易溶于水,密度比空气大;
(2)有毒,能与碱溶液反应;
(3)湿毛巾堵住口鼻,向高处跑;
(4)硫化氢能溶于水,有毒;
(5)B,D,氧气或二氧化碳或氢气,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(6)A,反应物状态是固体,反应条件是加热,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,E;
(7)可控制反应随时发生和停止;
(8)将长颈漏斗改为分液漏斗.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:选择题
| A. | 磷在空气中燃烧,有大量白雾生成 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 木炭在空气中燃烧,发出白光 | |
| D. | 铁丝在氧气中燃烧,生成一种黑色的固体四氧化三铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
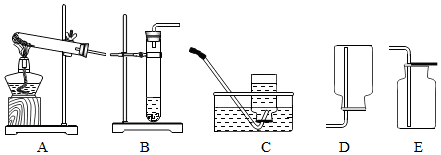
| 装置A | 装置B | |
| 反应状态 | 固体反应生成气体 | 固体和液体反应生成气体 |
| 反应条件 | 加热 | 无需加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
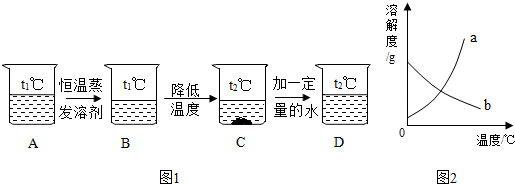
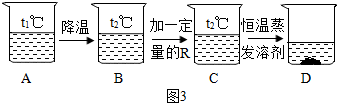
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
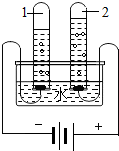 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
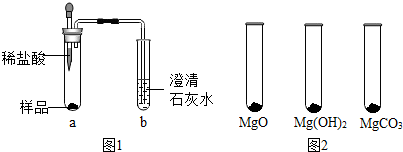
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com