

| | 样品 质量 | 装置及药品 总质量 | 装置及反应后物质 总质量 |
| 实验数据 | 144g | 394g | 378g |
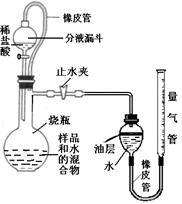


科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.向少许CaCO3粉末加人NaOH溶液充分振荡.无明显现象 |
| B.向少许CaCO3粉末加入过量稀盐酸充分振荡,粉末消失且有气泡产生 |
| C.向2颗蚕豆粒般石灰石固体加人3mL.蒸馏水,滴人酚酞试液片刻内不变红 |
| D.向少许CaCO3粉末加人3mL.蒸馏水充分振荡.滴入酚酞试液即变红 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 固体化台物________。 | | 盐酸过量 |
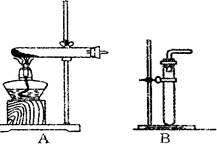
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题

| A.氢氧化钠溶液、二氧化碳 |
| B.酒精、氧气 |
| C.氢氧化钾溶液、氯化氢 |
| D.水、一氧化碳 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.从蜡烛上切一小块石蜡放入水中,石蜡浮在水面,说明石蜡的密度比水小 |
| B.取冷而干燥的小烧杯罩在蜡烛火焰上方,有水雾出现,说明石蜡中含有氢、氧元素 |
| C.在密闭容器中,蜡烛燃烧一段时间后熄灭,说明可燃物燃烧需要氧气 |
| D.用扇子可扇灭蜡烛火焰,说明将温度降至可燃物的着火点以下即可灭火 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| | Ba2+ | Ca2+ | Na+ | Cu2+ |
| OH– | 溶 | 微 | 溶 | 不 |
| CO32- | 不 | 不 | 溶 | 不 |
| Cl- | 溶 | 溶 | 溶 | 溶 |
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 取少量产物于试管中,加适量水中,振荡,静止 | | 燃烧产物中肯定有炭 |
| (2) | 取(1)所得少量上层清液,加入 | | |
| (3) | | | |


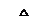 在步骤(3)中也可以通过加入 试剂的方法进行检验(任写一种与(3)中所加不同种类的试剂)。
在步骤(3)中也可以通过加入 试剂的方法进行检验(任写一种与(3)中所加不同种类的试剂)。查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
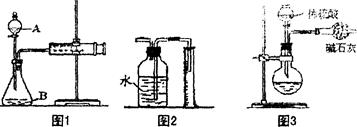

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com