
| ||
| △ |
| ||
| △ |
| ||
| 160 |
| 132 |
| 8.0g×x |
| 4.0g |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
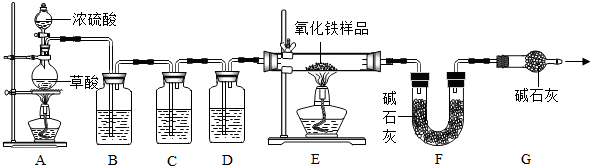
| A、用适量的稀盐酸除铁锈 Fe2O3+6HCl=2FeCl2+3H2O | ||||
B、用一氧化碳作燃料 C0+02
| ||||
C、高温煅烧石灰石制取生石灰 CaC03
| ||||
D、用红磷燃烧测定空气中氧气含量 S+O2
|
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.| 实验编号 | 1 | 2 | 3 |
| 实验前(g) | 2.00 | 2.00 | 2.00 |
| 实验后(g) | 0.43 | 0.44 | 0.45 |
查看答案和解析>>
科目:初中化学 来源: 题型:
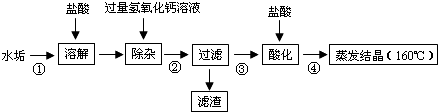
查看答案和解析>>
科目:初中化学 来源: 题型:
| 甲 | 乙 | 丙 | |
| 金属混合物的质量(g) | 10 | 10 | 20 |
| 稀硫酸质量(g) | 100 | 120 | 100 |
| 反应后余下固体质量(g) | 2 | 2 | 12 |
查看答案和解析>>
科目:初中化学 来源: 题型:
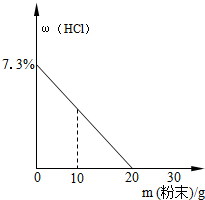 将混合均匀的Na2CO3和NaCl的粉末混合物不断加入100g稀盐酸中,溶液中HCl溶质的质量分数与加入粉末混合物的变化曲线如图所示.求:
将混合均匀的Na2CO3和NaCl的粉末混合物不断加入100g稀盐酸中,溶液中HCl溶质的质量分数与加入粉末混合物的变化曲线如图所示.求:查看答案和解析>>
科目:初中化学 来源: 题型:
 有些金属的氢氧化物有相似的化学性质,但物理性质却有所不同,如 Ca(OH)2、Ba(OH)2的溶解度就存在一定的差异,如表所示:
有些金属的氢氧化物有相似的化学性质,但物理性质却有所不同,如 Ca(OH)2、Ba(OH)2的溶解度就存在一定的差异,如表所示:| 温度/℃ | 0 | 40 | 80 | |
| 溶解度/g | Ca(OH)2 | 0.187 | 0.141 | 0.094 |
| Ba(OH)2 | 1.67 | 8.22 | 101.4 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
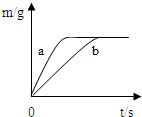 人类的生产、生活离不开金属.
人类的生产、生活离不开金属.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com