
 今年我市化学实验操作考察的实验之一是“高锰酸钾制取氧气”.现摘录某同学的实验过程如下:
今年我市化学实验操作考察的实验之一是“高锰酸钾制取氧气”.现摘录某同学的实验过程如下:分析 (1)根据实验室用高锰酸钾制氧气的反应原理写出反应化学方程式;
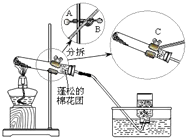
(2)根据铁架台上三个旋钮的不同作用进行调整试管的高度;铁夹处有3个,1个顶住铁架台竖直的铁杆,用于固定铁夹的高度;1个顶住铁夹后面的铁杆,用于固定铁夹的角度(试管口略向下倾斜);还有1个在铁夹上,用于夹紧试管;
(3)根据实验室检查装置的气密性的方法,漏气的原因进行解答;
(4)根据实验室制取氧气的装置,操作步骤 连→查→装→定→点→收→移→熄,及注意事项进行解答;
(5)根据实验室制取氧气的操作步骤,注意事项进行解答.
解答 解:(1)根据实验室用高锰酸钾制氧气的反应原理可知反应化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)根据铁架台上三个旋钮的不同作用,依据图示可知A可以调节试管的整个高度,故选A;
(3)根据检查装置气密性的方法:将导管插入水中,手握住试管,如果导管口有气泡冒出,松开手后,导管内有一段上升液柱,说明该装置气密性良好,证明不漏气;装置无破损,加热到高锰酸钾已大量分解,导管口仍未产生明显气泡,则可能造成的原因是:加入药品后橡皮塞没有塞紧;
故答案为:用手捂住大试管,导管口冒气泡,松手后导管口形成稳定的水柱;加入药品后橡皮塞没有塞紧;
(4)根据实验室制取氧气的装置,操作步骤、注意事项:
用排水法收集氧气:集气时导管伸入集气瓶的位置是 刚过集气瓶口,因为刚开始排出的是试管中的空气; 集气瓶充满水(不能有气泡)后倒放入水槽中;要等到气泡连续、均匀地放出时,再开始收集,否则收集到的氧气不纯,混有空气;
由此可知题中步骤:③集气瓶底部出现气泡;⑤导管口有气泡产生,立即用集气瓶进行收集;导致收集的氧气不纯;正确的方法是:③集气瓶底部不能出现气泡;⑤要等到气泡连续、均匀地放出时,再开始收集,故答案为:③⑤;
(5)根据实验操作:连→查→装→定→点→收→移→熄、及注意事项:实验完毕后,要先把导管移出水面,后熄灭酒精灯,防止因熄灭酒精灯而引起试管内温度降低,导致试管内压强骤然减小,水槽中的水沿导管进入试管,使试管炸裂;故答案为:倒吸(或大试管破裂).
答案:
(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)A;
(3)用手捂住大试管,导管口冒气泡,松手后导管口形成稳定的水柱;加入药品后橡皮塞没有塞紧;
(4)③⑤;
(5)倒吸(或大试管破裂).
点评 本题考查学生根据实验室氧气的制取的装置,步骤,注意事项进行分析解题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

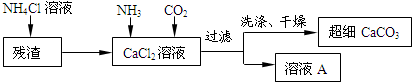
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
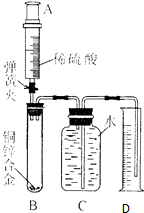 某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)
某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com