
【题目】某课外小组研究“影响 H2O2 生成 O2 反应速率的因素”的课题。通过查阅资料,提出如下猜想。
(提出猜想)催化剂和反应物浓度都会影响 H2O2 生成 O2 的反应速率。
(实验过程)实验装置如图。
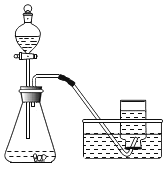
(实验操作)检查装置的气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶逸出的气体。
(实验记录)
实验编号 | Ⅰ | Ⅱ | Ⅲ |
反应物 | 5%H2O2 50mL | 5%H2O2 50mL | 3%H2O2 50 mL |
加入固体 | 0.5g CuO | 0.5g MnO2 | 0.5g MnO2 |
收集等体积O2所需时间 | 105s | 45s | 78s |
充分反应后,将实验Ⅱ中剩余物质里的 MnO2提取的方法是_____。
(实验结论)该探究过程得出的结论是_____。
(反思评价)H2O2 在常温加入 MnO2 后反应速率加快。小敏同学提出,为了更好地证明 MnO2 对 H2O2 生成O2反应速率的影响,还应该增加一组对比实验。该实验选用的药品和用量为_____。
(实验拓展)小敏同学发现用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象。造成这种结果的可能原因是_____。
【答案】过滤/(过滤、洗涤、干燥) 催化剂的种类和反应物H2O2的浓度都会影响反应速率 5%H2O2 50mL(不加催化剂)/3%H2O2 50mL(不加催化剂) 氧气不纯净/铁丝生锈/火材梗太长过多地消耗了瓶内氧气(合理即可)
【解析】
过氧化氢在催化剂催化作用下生成水和氧气,铁在氧气中点燃生成四氧化三铁。
[实验记录]二氧化锰不溶于水,故充分反应后,将实验Ⅱ中剩余物质里的 MnO2提取的方法是过滤/(过滤、洗涤、干燥)。
[实验结论]催化剂能加快反应速率,过氧化氢的浓度越大,反应速率越快,故该探究过程得出的结论是催化剂的种类和反应物H2O2的浓度都会影响反应速率。
[反思评价]H2O2 在常温加入 MnO2 后反应速率加快。小敏同学提出,为了更好地证明 MnO2 对 H2O2 生成O2反应速率的影响,应该设置对照实验,前面均加催化剂,则实验不加催化剂做对照,故该实验选用的药品和用量为5%H2O250mL(不加催化剂)/3%H2O250mL(不加催化剂)。
[实验拓展]氧气不纯净,铁丝生锈等均不燃烧,用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象,造成这种结果的可能原因是氧气不纯净/铁丝生锈/火材梗太长过多地消耗了瓶内氧气。


科目:初中化学 来源: 题型:
【题目】小兵带回一瓶浑浊山泉水,他在实验室模拟自来水厂净水过程,最终制成蒸馏水,流程如图:
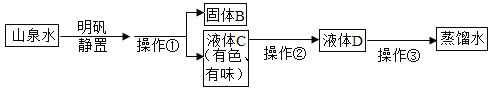
(1)操作①的名称是_________(填操作名称),实验室进行该操作时玻璃棒的作用是_________,该操作需要的玻璃仪器除玻璃棒外,还需要_________;(填仪器名称)若经过操作①后,所得液体C中仍有浑浊,其原因可能是_________(填序号);
a漏斗内的滤纸有破损 b漏斗下端未靠在烧杯内壁 c漏斗内液面高于滤纸的边缘
(2)操作②主要是除去一些异味和色素,应选用的物质是__________________(填名称);
(3)取少量液体D于试管中,加入少量肥皂水,振荡,发现有较少泡沫,说明液体D是_________,(填“硬水”或“软水”),操作③其净水效果最佳,是_________(填操作名称)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】叶酸对防癌抗癌有积极作用,其化学式为C19H19N7O6,下列有关叶酸的说法中正确的( )
A.叶酸属于氧化物
B.叶酸中碳、氢、氮、氧四种元素的质量比为19:19:7:6
C.叶酸中氮元素的质量分数大于氧元素的质量分数
D.叶酸由19个碳原子、19个氢原子、7个氮原子和六个氧原子构成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A.质量相等的CO与CO2中碳元素质量比为7:11
B.NO、NO2、N2O3中氮元素质量分数最大的是二氧化氮
C.含氨质量分数为16.8%的碳酸氢铵(NH4HCO3)化肥是纯净物
D.160g的Fe2O3中含有铁元素的质量为112g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小宇查阅资料得知:氯酸钾在二氧化锰、氧化铁等物质作催化剂条件下可生成氯化钾和氧气。于是,他对影响氯酸钾分解的因素及催化剂的效果产生了探究兴趣。
(提出问题)氧化铁是否比二氧化锰催化效果更好?
(设计实验)小宇以生成等体积的氧气为标准,设计了下列几组实验。
序号 | KClO3 | 其它物质的质量 | 温度 | 收集氧气的体积 | 反应时间 |
① | 10.0g | 无 | 330℃ | 100mL | t1 |
② | 10.0g | 氧化铁1.5g | 330℃ | 100mL | t2 |
③ | 10.0g | 二氧化锰1.5g | 330℃ | 100mL | t3 |
④ | 10.0g | 二氧化锰xg | 380℃ | 100mL | t4 |
(结论与反思)
(1)若t1________t2(选填“>”、“=”或“<”),说明氧化铁能加快氯酸钾的分解速率。若要确定氧化铁是氯酸钾分解反应的催化剂,还需探究反应前后氧化铁的________和________不变。
(2)若t2>t3,说明氧化铁对氯酸钾分解的催化效果比二氧化锰________(填“强”或“弱”)。
(3)写出实验④所涉及反应的化学方程式__________________。
(4)实验④中MnO2的质量x为________g,若t3 > t4,则化学反应速率与温度的关系是______________。
(5)氯酸钾的分解速率可能还与_____________________因素有关,需设计实验进一步证明。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置,结合所学化学知识回答下列问题。
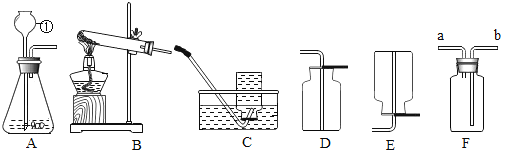
(1)请写出题中标号仪器的名称:①________,实验室用高锰酸钾制取氧气,可选用的发生装置为________(选填装置编号,下同),收集氧气可选择D装置其原因是________,发生反应的化学方程式为________。
(2)用大理石和稀盐酸制取CO2时,应选用的发生装置是________。发生反应的化学方程式为________ ,若用F装置收集CO2气体应从________处进入(选填导管口编号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图回答问题:
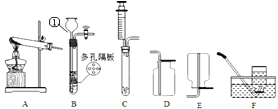
(1)写出图中标号仪器名称:①_____;
(2)实验室用氯酸钾制取并收集较纯净的氧气应选用的装置是_____(填序号,下同),反应的符号表达式为_____。
(3)某同学提出只要将上述A装置和下图所示装置相连接,就可收集并测量生成的氧气的体积,则正确的连接顺序是:A装置的导管出口→(____)→(____)→a(填接口字母)。
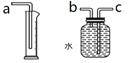
(4)实验室采用锌粒和稀硫酸反应制取氢气,要求实验中产生平稳的氢气流,则适合的制取装置的组合是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锌元素是人体健康必需的微量元素,葡萄糖酸锌是一种常用的补锌剂。锌缺乏容易造成发育障碍,使人体免疫功能低下。如图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答:

(1)葡萄糖酸锌的相对分子质量为______。
(2)葡萄糖酸锌中C:H:O:Zn的质量比为______。
(3)每支葡萄糖酸锌口服液中含葡萄糖酸锌的质量是______ mg。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com