
 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将90.8克的盐酸加入到12.5g水垢中,完全反应后产生CO2气体的情况如图所示.
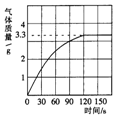
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将90.8克的盐酸加入到12.5g水垢中,完全反应后产生CO2气体的情况如图所示.分析 根据生成的二氧化碳的质量和对应的化学方程式求算碳酸钙的质量,进而求算对应的质量分数.同时根据碳酸钙的质量求算氢氧化镁的质量,结合对应的化学方程式求算氯化镁的质量,进而求算对应的质量分数.
解答 解:由图可知生成的二氧化碳的质量为3.3g.设该石灰石样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{44}$=$\frac{x}{3.3g}$
x=7.5g
水垢中碳酸钙的质量分数为$\frac{7.5g}{12.5g}$×100%=60%
氢氧化镁的质量为12.5g-7.5g=5g
设生成的氯化镁的质量为y
Mg(OH)2+2HCl=MgCl2+2H2O
58 95
5g y
$\frac{58}{95}$=$\frac{5g}{y}$
y≈8.2g
完全反应后溶液中MgCl2的质量分数为$\frac{8.2g}{12.5g+90.8g-3.3g}$×100%=8.2%
答:(1)水垢中碳酸钙的质量分数是60%.
(2)假设水垢中除碳酸钙和氢氧化镁外,不含有其它杂质,完全反应后溶液中MgCl2的质量分数为8.2%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 溶液一定是无色透明的液体 | |
| B. | 溶液的体积等于溶质和溶剂体积之和 | |
| C. | 溶液是均一、稳定的混合物 | |
| D. | 溶质只能是固体或气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20℃时,100g水中能溶解氯化钠36g,形成136克氯化钠的饱和溶液 | |
| B. | 20℃时,100g氯化钠饱和溶液中含氯化钠36g | |
| C. | 20℃时,氯化钠饱和溶液中水与氯化钠的质量比为64:36 | |
| D. | 20℃时,将36g氯化钠溶解于64g水中,所得溶液为该温度下氯化钠的饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 名称 | 颜色、气味 | 熔点(℃) | 沸点(℃) | 25℃水中溶解度(g/L) | 标况下密度 (g/L) |
| NH3 | 无色、刺激性 | -77.7 | -33 | 456 | 0.6942 |
| H2 | 无色、无味 | -259.2 | -253 | 0.0015 | 0.0899 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
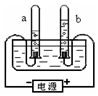
| A. | a试管中收集到的是一种可燃性气体 | |
| B. | 该实验能证明水是由氢元素和氧元素组成 | |
| C. | b试管中收集到的是氧气 | |
| D. | a、b两试管内收集到的气体的质量比约为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO2+CaCl2+H2O═CaSO3↓十2HCl | B. | SO2+2NaOH═Na2SO3+H2O | ||
| C. | Na2SO3+CaCl2=CaSO3↓+2NaCl | D. | H2SO3+2NaOH=Na2SO3+2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
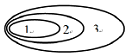 如表中1、2、3各项之间能构成如图包含关系的是( )
如表中1、2、3各项之间能构成如图包含关系的是( )| 编号 选项 | 1 | 2 | 3 |
| A | 金属 | 水银 | 合金 |
| B | 酸 | 化合物 | 纯净物 |
| C | 中和反应 | 复分解反应 | 置换反应 |
| D | 氧化物 | 碱 | 化合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com