
(12分)水是生命之源,是自然界中重要的物质。
Ⅰ.温泉的利用是人们开发地热的一种形式,南京汤山温泉具有悠久的文化。
(1)清澈的温泉水是 (填“纯净物”或“混合物”)。
(2)净化温泉水的过程中,会使用到活性炭,主要是利用其 作用。
(3)鉴别温泉水是硬水还是软水需加入的试剂是 。
Ⅱ.海水是巨大的资源宝库。海水晾晒可得到粗盐,已知某粗盐样品中除泥沙外还含有Na2SO4、MgCl2、CaCl2等杂质。实验室提纯流程如下: 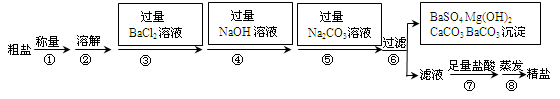
(1)用托盘天平称量10.2g粗盐样品时,若指针偏向左边,则表示(填字母序号) 。
| A.右盘重,砝码轻 | B.右盘轻,样品少 |
| C.左盘重,样品多 | D.左盘轻,砝码重 |
Ⅰ.(1)混合物 (2)吸附 (3)肥皂水 Ⅱ.(1)C (2)2NaOH+ MgCl 2==Mg(OH)2↓ +2NaCl;(3)除尽氯化钡和氯化钙 (4)除去过量的NaOH和Na2CO3(5)112.5Kg
解析试题分析:Ⅰ.(1)清澈的温泉水是混合物;(2)净化温泉水的过程中,会使用到活性炭,主要是利用其吸附性(3)鉴别温泉水是硬水还是软水需加入的试剂是肥皂水;Ⅱ.(1)用托盘天平称量10.2g粗盐样品时,若指针偏向左边,则表示C.左盘重,样品多;(2)第④步操作是加入过量的氢氧化钠,除去镁离子的过程,发生反应的化学方程式是2NaOH+ MgCl 2==Mg(OH)2↓ +2NaCl;(3)第⑤步操作加入碳酸钠溶液,目的是除尽过量氯化钡和含有氯化钙;(4)在第⑦步操作中,向滤液中滴加足量盐酸的目的是除去过量的NaOH和Na2CO3;Ⅲ.(5)解:设:需要水的质量为x 0.5分
2H2O 通电2H2 ↑+O2 ↑ 1分
36 32
x 100kg 1分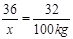
1分
x=112.5kg 1分
答:所需氯化钠溶液的质量是112.5kg 0.5分
考点:水的有关知识、化学方程式的计算


科目:初中化学 来源: 题型:计算题
(7分)在一烧杯中盛有60.2gBaCO3和BaCl2的粉末状混合物,向其中加入188.8g水使混合物中可溶物完全溶解,然后向其中逐滴加入溶质质量分数为10%的稀盐酸至146g时恰好反应完全,请根据题意回答问题:
(1)在滴加盐酸过程中观察到的明显实验现象是 。
(2)当盐酸滴加至140g时,烧杯中溶液里含有溶质的是 。(写化学式)
(3)计算恰好反应完全时烧杯中所得不饱和溶液的质量。(结果精确到0.1g)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)硫代硫酸钠(Na2S2O3)是一种用途广泛的物质。某硫代硫酸钠样品中含有少量的硫酸钠。现取16 g该样品放入烧杯中,加入113.6 g一定溶质质量分数的稀硫酸恰好完全反应,得到120 g硫酸钠不饱和溶液。
发生反应的化学方程式为:Na2S2O3 + H2SO4=== Na2SO4 + H2O + S↓+ SO2↑
请计算:
(1)样品中硫代硫酸钠(Na2S2O3)与硫酸钠的质量比。
(2)所得溶液中溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(3分)某化工厂生产的氧化亚铜(Cu2O)产品中常含有10%的金属铜。现准备用40 t该产品生产10%的硫酸铜溶液。已知:Cu2O+H2SO4===CuSO4+Cu+H2O
求:所需溶质质量分数为20%的稀硫酸质量和加水的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题: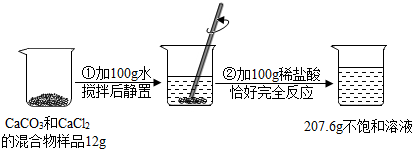
(1)实验所用稀盐酸的溶质的质量分数为 7.3%.
(2)计算原混合物样品中CaCl2的质量(写出计算过程).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
小玉同学在实验室发现了一瓶敞口放置的过氧化氢溶液,他认为该溶液中溶质的质量分数减小了,需要重新测定并更换试剂瓶的标签。他做了如下实验:称量该溶液34.0g倒入烧杯中,然后向其中加入少量二氧化锰,直到不再放出气体后,再称量烧杯中混合物的质量,称量结果为33.7g。
(1)该溶液溶质的质量分数减小的理由是__________________________。
(2)若二氧化锰的质量是0.5g,则生成的气体的质量为___________g。
(3)计算该瓶溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某工厂利用废硫酸和废铁屑起反应来制取硫酸亚铁。现有废硫酸9.8 t(H2SO4的质量分数为10%)与足量的铁屑起反应,理论上可生产FeSO4的质量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com