
在Fe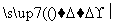 FeSO4
FeSO4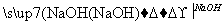 Fe(OH)2
Fe(OH)2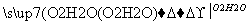 Fe(OH)3的各步转化中,所属的基本反应类型不包括( )
Fe(OH)3的各步转化中,所属的基本反应类型不包括( )
A.化合反应 B.复分解反应
C.置换反应 D.分解反应
科目:初中化学 来源: 题型:
硒是人体必需的一种微量元素,严重缺硒有 可能诱发皮肤疾病。已知
可能诱发皮肤疾病。已知
硒的原子序数为34,质子数与中子数之和为79。下列有关硒原子的说法中,不正确的是( )
A.核电荷数为79 B.核外电子数为34
C.质子数为34 D.中子数为45
查看答案和解析>>
科目:初中化学 来源: 题型:
近几年“纸火锅”(如图)逐渐流行起来.“纸火锅”是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧.对此现象,下列解释合理的是()

|
| A. | 纸张不是可燃物,不能燃烧 |
|
| B. | 水蒸发时吸收热量,温度达不到纸张的着火点 |
|
| C. | 纸张被水浸湿,导致着火点降低 |
|
| D. | 空气不充足,纸张不会燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:
除去下列各物质中混有的少量杂质,所用试剂、方法正确的是( )
| 序号 | 物质 | 杂质 | 试剂、方法 |
| A | CO2 | CO | 点燃 |
| B | Fe粉 | Cu粉 | 稀盐酸,过滤 |
| C | MgCl2溶液 | 盐酸 | 适量的氢氧化钠溶液 |
| D | FeSO4溶液 | CuSO4 | 过量铁粉,过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:
某化学兴趣小组进行铁生锈的实验探究活动.
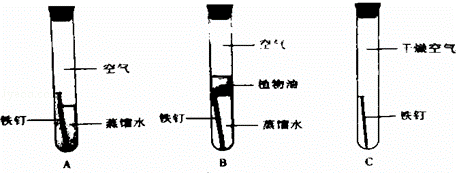
【探究一】铁生锈的条件
(1)该兴趣小组将洁净无锈的铁钉分别置于如图所示装置中,经过一段时间观察 ,(填装置序号)装置中出现了明显的锈迹.
他们的结论:铁生锈是因为铁与空气中的 等发生了化学反应.
(2)甲同学提出了疑问:空气中的氮气、二氧化碳没有参与铁的生锈过程吗?请设计实验为甲同学释疑. ,观察并记录现象即可证明.
【探究二】影响铁生锈速率快慢的因素
乙同学说:妈妈常说菜刀沾有盐水生锈更快.这种说法对吗?同学广泛查阅资料.
资料一:导电性强的溶液都可加速铁的生锈.
资料二:海上航行的轮船在与海水接触的部分镶嵌一锌块,能有效降低钢材被腐蚀的速率.
(3)将上述A装置中的蒸馏水改为下列液体中的 ,可使铁生锈的速率加快.
a、硫酸钠溶液 b、无水乙醇 C、蔗糖溶液
(4)一些铁制品表面覆盖了某些涂层.不同的涂层被破坏后,铁生锈的速率不同.你认为下列 涂层破坏后,铁生锈的速率较快.
a、镀锌铁 b、镀锡铁
(5)一些建筑的大门刷上了一层银白色的金属,你认为该金属可能是 .
a、银粉 b、铜粉 c、镁粉
【交流与思考】
(6)写出一种防止铁生锈的方法 .
查看答案和解析>>
科目:初中化学 来源: 题型:
置换反应是中学化学反应的基本反应类型之一。
已知:化合物A+单质B→化合物C+单质D。试回答:
(1)若D为氢气,A为稀硫酸,则B的选择应满足的条件是__ __;
(2)若D为铜,化合物A的化学式可能为__ __;
(3)已知在高温条件下碳与水蒸气可反应生成一氧化碳和氢气(水煤气的主要成分),写出该反应的化学方程式_ __; 若家中使用煤气做燃料,一旦泄漏,下列应急措施可行的有__ __(填字母序号)。
A.检查并关闭气源阀门
B.轻轻打开门窗通风
C.立即打开抽油烟机排气
(4)非金属单质也具有类似金属与盐溶液之间发生置换反应的规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来。如在溶液中可发生下 列反应:
列反应:
Cl2+2NaBr===2NaCl+Br2
I2+Na2S===2NaI+S↓
Br2+2KI===2KBr+I2↓
由此可判断:
①四种单质S、Cl2、I2、Br2中非金属活动性最强的是__ __,最弱的是__ __。
②下列化学方程式书写错误的是__ __(填字母序号)。
A.Cl2+2NaI===2NaCl+I2↓
B.Br2+Na2S===2NaBr+S↓
C.I2+2KBr===2KI+Br2
(5)在化学反应中,物质所含元素的化合价 发生变化的反应就是氧化还原反应,置换反应__属于__(填“属于”或“不属于”)氧化还原反应。
发生变化的反应就是氧化还原反应,置换反应__属于__(填“属于”或“不属于”)氧化还原反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
今年我市的化学实验操作考试有“制取并收集一瓶二氧化碳”的考题。

(1)指出标号①的仪器名称__ __;
(2)实验室制取二氧化碳选用的发生装置和收集装置为__(填序号),反应的化学方程式为__ __。
(3)化学兴趣小组的同学对反应后废液中溶质的成分进行进一步探究。
【提出问题】废液中的溶质含有哪些物质?
【猜想与假设】猜想Ⅰ:溶液中的溶质只有CaCl2;
猜想Ⅱ:废液中的溶质有__ __。
【进行实验】兴趣小组的同学取废液进行了以下实验,请你与他们一起完成下列实验报告。
| 实验操作 | 实验现象 | 实验结论 |
| 取少量反应后的废液于试管中,向其中加入Na2CO3溶液至过量 | ||
| 只有_ | 猜想Ⅰ正确 | |
| 先_产生气泡_ | ||
| 后_产生沉淀_ | 猜想Ⅱ正确 |
如果猜想Ⅰ正确,有关反应的化学方程式为:___;
【反思拓展】如果猜想Ⅱ正确,要使废液中只含有CaCl2,正确的处理方法是加入过量的__ __。
查看答案和解析>>
科目:初中化学 来源: 题型:
图中:A、B、C、D、E、F、G是初中化学常见的物质,其中A为单质,B为氧化物,C是大理石的主要成分,C和F属于不同类别的物质,D和E是配制农药波尔多液的两种原料。“—”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质。
请回答:

(1)D和E发生反应的基本反应类型为_ _。
(2)完成下列化学方程式:
①A→B的化学方程式_ _。
②B→C的化学方程式_ _。
(3)物质F可以是_(具体写两种不同类别的物质)。
查看答案和解析>>
科目:初中化学 来源: 题型:
做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和 两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变 色 | 猜想(3)成立 |
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是 .兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液? (填“能”或“不能”)
(2)乙同学的实验中铝片与 氢氧化钠 溶液发生了反应,请写出铝与该溶液发生反应的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com