
| A. | 工业三废的任意排放 | B. | 植树造林,修建水库 | ||
| C. | 农药和化肥的广泛使用 | D. | 生活垃圾和污水的任意倾倒 |
科目:初中化学 来源: 题型:实验探究题
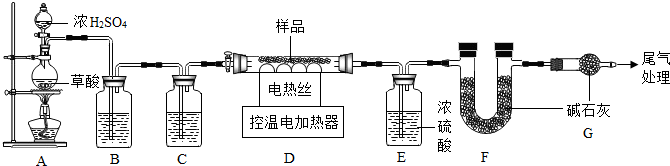
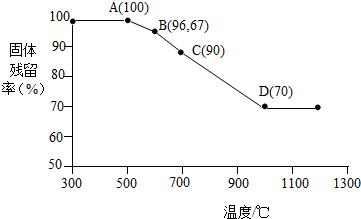
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | TI | B. | tI | C. | Ti | D. | ti |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 钠原子失去电子后变成钠离子 | B. | 氯离子失去电子后不能变成氯原子 | ||
| C. | 原子的质量主要集中在原子核上 | D. | 化学变化中原子不能再分 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
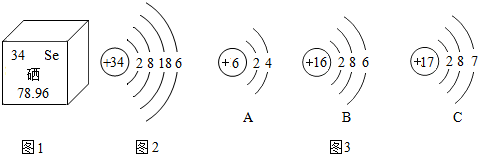
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

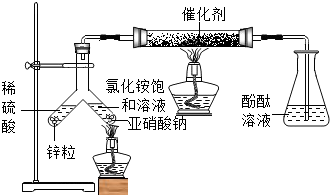
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com