
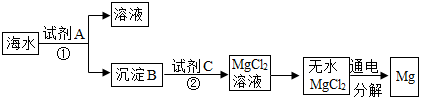
分析 (1)氯化镁转化为氢氧化镁需要加入碱液,验证MgCl2已完全转化为Mg(OH)2的方法是取滤液滴入NaOH溶液是否有沉淀生成;
(2)利用题目所给的信息结合书写化学方程式的原则进行书写;
(3)根据海水中氯化镁的浓度低进行解答.
解答 解:(1)氯化镁转化为氢氧化镁需要加入碱液以提供氢氧根,此处选择过量的氢氧化钠进行反应,目的是让所取海水中的氯化镁全部转化为氢氧化镁沉淀;验证MgCl2已完全转化为Mg(OH)2的方法是取滤液滴入NaOH溶液,若无沉淀产生,则已完全转化.氢氧化镁属于沉淀,需要加入酸溶解,所以变为氯化镁的方法是加入稀盐酸,所以试剂C是稀盐酸;故答案为:过量氢氧化钠溶液;让所取海水中的氯化镁全部转化为氢氧化镁沉淀;取滤液滴入NaOH溶液,若无沉淀产生,则已完全转化;稀盐酸;
(2)由题中可知反应产物,再结合化学反应方程式的书写原则书写方程式.故答案为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
(3)海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:海水中氯化镁的浓度低.故答案为:海水中氯化镁的浓度低.
(1)NaOH 或 Ca(OH)2或 CaO(合理即可); 让所取海水中的氯化镁全部转化为氢氧化镁沉淀;静置,往上层清液中继续加试剂A,不再产生沉淀;盐酸
(2)MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑
(3)海水中MgCl2含量太低(合理即可).
点评 此题是对海水中物质的提纯应用的考查,主要是利用了酸碱盐之间的相关反应,解决了物质的相关转化,是复分解反应发生条件的具体应用.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钾溶液 | 硝酸银溶液 | |
| 稀盐酸 | 示例:①能反应 | ②不能反应 | ③能反应 | ④能反应 |
| 判断依据 | 示例:有水生成 | 无气体或沉淀或水生成 | 有气体生成和水 | 有沉淀生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
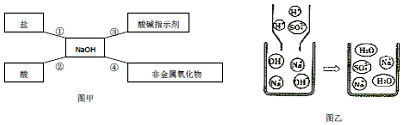
 如图所示的是海水淡化膜分离技术.对淡化膜右侧的海水加压,在其左侧得到淡水.其原理是海水中的水分子可以透过淡化膜,而其他各种离子不能透过.请回答:
如图所示的是海水淡化膜分离技术.对淡化膜右侧的海水加压,在其左侧得到淡水.其原理是海水中的水分子可以透过淡化膜,而其他各种离子不能透过.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com