
合金是重要的金属材料.
(1)下列物品所使用的主要材料属于合金的是 (填字母,下同).
A.青花瓷茶杯 B.水银温度计 C.不锈钢水槽
(2)根据含碳量不同,铁的合金可分为生铁和 ,将生铁投入到盛有稀盐酸的试管中,表明反应已完全的现象是 ,试管中有黑色不溶物是 .
(3)黄铜是铜锌合金,将纯铜片和黄铜片互相刻划(如图1所示),纯铜片上留下明显的划痕,说明 .
(4)黄铜渣中约含 Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如图2(杂质不溶于水、不参与反应):
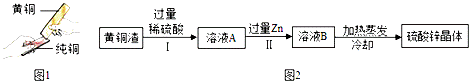
已知:ZnO+H2SO4═ZnSO4+H2O;CuO+H2SO4═CuSO4+H2O.
下列说法正确的是 .
a.Ⅰ、Ⅱ中的操作均包含过滤
b.溶液A中ZnSO4 的质量大于CuSO4
c.溶液A的质量小于溶液B.
| 合金与合金的性质;金属的化学性质;生铁和钢.. | |
| 专题: | 金属与金属材料. |
| 分析: | (1)合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;合金具有以下特点:①一定是混合物;②合金中至少有一种金属等. (2)生铁和钢是铁的重要合金,其区别在于含碳量的不同,铁与盐酸反应可生成氢气,据此回答问题即可. (3)合金要比组成它的纯金属的硬度大; (4)根据金属与酸、盐的溶液反应的规律进行分析解答; |
| 解答: | 解:(1)青花瓷不含有金属,故不是合金;水银温度计的主要材料是水银,水银是金属单质,不是合金;不锈钢是铁的合金,含有铁和碳,是合金; (2)钢和生铁是铁的主要合金,铁的活动性在氢前铁,所以可以与盐酸反应生成氢气,同时生成氯化亚铁,表明反应已完全的现象是无气泡产生,即为铁已完全反应,生铁中的碳不能与盐酸反应,所以会以黑色不溶物的形式存在于溶液中. (3)将纯铜片和黄铜片互相刻画,纯铜片上留下明显的划痕,说明黄铜的硬度比纯铜的硬度大; (4)由图可知,操作Ⅰ过滤后得铜,操作Ⅱ过滤是除去锌; 因氧化锌的质量大于氧化铜,另外锌也能和硫酸反应生成硫酸锌,而铜和硫酸不反应,故溶液A中硫酸锌的质量大于硫酸铜; 溶液A加入锌后,反应的化学方程式分别为:H2SO4+Zn═ZnSO4+H2↑;CuSO4+Zn═ZnSO4+Cu;对反应H2SO4+Zn═ZnSO4+H2↑分析可知,每65份质量的锌进入溶液,从溶液中出来2份质量的氢气,使得溶液质量增加,对于反应CuSO4+Zn═ZnSO4+Cu来说,每65份质量的锌进入溶液,从溶液中析出64份质量的铜,也使得溶液质量增大;故溶液A的质量小于溶液B; 故答案为:(1)C; (2)钢; 无气泡产生; 碳; (3)黄铜的硬度比纯铜的硬度大;(4)abc. |
| 点评: | 本题重点考查了合金的相关知识及金属活动性顺序及其应用,了解相关知识即可正确解答. |


科目:初中化学 来源: 题型:
空气是一种宝贵的自然资源。
(1)对空气的成分:①氧气 ②氮气 ③稀有气体 ④二氧化碳及其它气体和杂质。
按体积计算,由多到少的排列顺序正确的是
A.①②③④ B.②①③④ C.①②④③ D.②①④③
(2)下列事实说明空气中含有哪些成分(填名称)
①酒精在空气中可以燃烧说明空气中含有
②酥脆的饼干露置于空气中变软说明空气中含有
③澄清的石灰水在空 气中放置,其表面生成一层白膜说明空气中含有
气中放置,其表面生成一层白膜说明空气中含有
(3)目前我国对城市空气质量监测项目中,一般不考虑的是
A.二氧化碳 B.二氧化氮 C.二氧化硫 D.可吸入颗粒物
查看答案和解析>>
科目:初中化学 来源: 题型:
下列图象不能正确反映其对应变化关系的是( )
|
| A. |
用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 |
|
| B. |
一定质量的红磷在密闭容器中燃烧 |
|
| C. |
向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 |
|
| D. | 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
一节一号干电池烂在地里,能使1m2的土壤永久失去利用价值;一粒纽扣电池可使600t水受到污染,相当于一个人一生的饮水量.许多有识之士正在研究废旧电池的有效回收再利用技术.图1为干电池示意图.
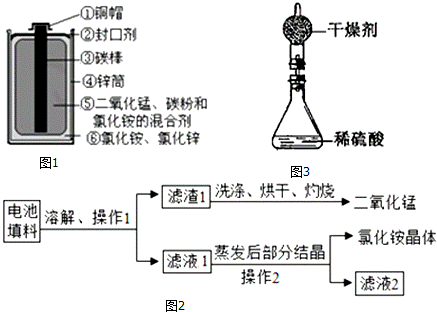
【物质归类】将回收的废干旧电池进行分离归类
(1)可以得到的单质有(用化学式表示,下同) ,
氧化物有 .
某化学兴趣小组回收利用废旧干电池并进行相关实验探究.
【实验探究1】回收填料中的二氧化锰和氯化铵
查阅资料:干电池示意图中⑤和⑥为填料,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如图2所示.
(2)操作1和操作2的名称都是 ,该操作中玻璃棒的作用是 .
(3)灼烧滤渣l的目的是 .
【实验探究2】探究影响锌与稀硫酸反应快慢的因素
(4)反应过程中,用前10min内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如下表.
| 实验编号 | 试剂 | 前10 min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30 mL 30% | 564.3 |
| b | 含杂质的锌 | 30 mL 30% | 634.7 |
| c | 纯锌 | 30 mL 20% | 449.3 |
| d | 纯锌 | 40 mL 30% | 602.8 |
①比较实验a和实验b,可以得到的结论是 .
②为了研究硫酸浓度对反应快慢的影响,需比较实验 和实验 (填编号).
③控制其他条件相同,需控制的条件是 (例举一种条件即可).
【实验探究3】利用锌皮和稀硫酸制取氢气,并测定锌皮中锌的质量分数
(5)制取氢气的实验操作有:
a.收集气体;b.向锥形瓶里装锌皮;c.连接仪器,检查装置气密性;d.向长颈漏斗中注入稀硫酸;e.装配仪器.
正确的操作顺序为 .
(6)测定锌皮中锌的质量分数:已知该锌皮中含有少量杂质铁,将该锌皮放入如图3所示的盛有稀硫酸的锥形瓶中,多次实验后,取平均值所得数据如表:
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌皮质量 | |
| 342.1g | 16g | 357.7g |
若不考虑干燥剂吸收空气中的水蒸气,请分析计算:
①根据质量守恒定律求生成氢气的质量为 g.
②该合金中锌的质量为 g,锌皮中锌的质量分数为 %.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com