
 如图是甲、乙两种物质的溶解度曲线,请回答下列问题:
如图是甲、乙两种物质的溶解度曲线,请回答下列问题:分析 (1)两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;
(2)由图可知:乙的溶解度随着温度的升高而降低;
(3)甲的溶解度随着温度的升高而增大,随着温度的降低而减小,故要使甲从其浓溶液中析出,通常可采用降温结晶的方法;
(4)t2℃时,甲种物质的溶解度为90g>65g,乙种物质的溶解度小于65g;分别将甲、乙两种物质的饱和溶液降温到t1℃,同质量的甲、乙两种物质的溶液所含溶质质量不同,甲大于乙;所以甲溶液的溶质质量分数大于乙溶液的溶质质量分数;
(5)①根据水的污染源分析造成水体污染的做法;
②根据反应原理写出反应的方程式.
解答 解:
(1)由图中甲乙两物质的溶解度曲线可以知道,在t1℃时,甲、乙物质的溶解度曲线相交于一点.所以,t1℃时,甲物质的溶解度等于乙物质的溶解度;
(2)由图可知:乙的溶解度随着温度的升高而降低;
(3)甲的溶解度随着温度的升高而增大,随着温度的降低而减小,故要使甲从其浓溶液中析出,通常可采用降低温度的方法;即降温结晶或冷却热饱和溶液;
(4)t2℃时,甲种物质的溶解度为90g>65g,乙种物质的溶解度小于65g;分别将甲、乙两种物质的饱和溶液降温到t1℃,同质量的甲、乙两种物质的溶液所含溶质质量不同,甲大于乙;所以甲溶液的溶质质量分数大于乙溶液的溶质质量分数;
(5)①A.生活污水直接排放,会造成水的污染;
B.工业废水处理后排放,不会造成水的污染;
C.磷的大量排放会造成水体的富营养化,禁止使用含磷洗衣粉,能防止水的污染;
D.合理使用化肥、农药,不会造成水的污染;
②Ca(HCO3)2受热分解生成水、难溶性的CaCO3,并放出一种能使澄清石灰水变浑浊的二氧化碳气体,化学方程式为:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O;
故答案为:
(1)t1;
(2)乙;
(3)冷却热饱和溶液(或降温结晶);
(4)大于;
(5)①A;②Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O.
点评 本题考查了从溶解度曲线图上读取信息、分析及获取信息的能力.从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同,以及方程式的书写等知识.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:解答题
| 温度/℃ | O | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | O.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
| A. | 表中m的值为2.8 | |
| B. | X中氧元素的质量为1.6g | |
| C. | 增加氧气的量可以减少X的生成 | |
| D. | 物质X一定含有1.2g碳元素,可能含有氢元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用胶头滴管,为了节约药品,剩余的药品挤回原瓶,然后再清洗放回原处 | |
| B. | 排空气法收集氧气,为了便于空气的排出和氧气的验满,把毛玻片取下 | |
| C. | 取用固体后,用过的镊子或药匙要立刻用纸擦拭干净,以便下次使用 | |
| D. | 称量固体药品,校零后,将固体药品放在左盘上称量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2O与H2O2的化学性质不同的原因是原子个数不同 | |
| B. | 金刚石和石墨的物理性质差异大的原因是碳原子个数不同 | |
| C. | 生铁与钢的性能不同的原因是含碳量不同 | |
| D. | 稀盐酸与稀硫酸的化学性质相似的原因是都含有酸根离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 序号 | 实验操作 | 实验现象 |
| ① | 收集两瓶气体,盖好玻璃片,停止加热,向其中一瓶迅速倒入少量澄清石灰水,盖好振荡. | 无明显现象. |
| ② | 将另一瓶气体点燃,待火焰熄灭后,迅速倒入少量澄清石灰水,盖好振荡. | 气体安静燃烧,火焰呈蓝色,澄清石灰水变浑浊. |
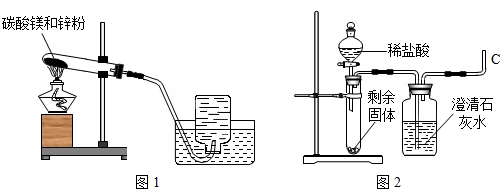
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 化肥的种类、鉴别及使用 | 化学应用 | ||
A | CO(NH2)2、(NH4)2SO4和NaNO3均可用作氮肥 从外观上可区分硫酸钾和磷矿粉两种肥料 给农作物施肥时同时施用草木灰和碳酸氢铵以提高肥效 | B | 用肥皂水检验硬水和软水 用食醋清洗家用瓷器上的水垢 用燃烧后闻气味的方法鉴别衣服面料是蚕丝还是合成纤维涤纶 |
| 食品安全 | 能源与环境 | ||
C | 用硫磺熏制白木耳、粉丝等食品 用小苏打作焙制糕点的发酵粉 除鱼胆汁苦味(酸性)--纯碱溶液浸泡 | D | 煤、石油燃烧--无污染 车用乙醇汽油--减少污染 氢能--无污染 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com