25.(2007?哈尔滨)实验室里同学们要配制一定溶质质量分数的氯化钙溶液.药品柜中可供选择的药品只有氢氧化钙、氧化钙、碳酸钙和硝酸钙四种固体及一定溶质质量分数的稀盐酸.同学们交流讨论后,选择了一种固体药品并称取15g加入烧杯中,再向其中加入105.4g稀盐酸,充分反应后过滤,得到5g固体和111g氯化钙溶液(实验中物质损耗忽略不计),并将上述配好的氯化钙溶液倒人贴有相应标签的试剂瓶中.请回答下列问题:
(])同学们选择的固体药品是;
(2)请写出题中发生反应的化学方程式;
(3)请根据已知条件列出求解生成氯化钙质量(X)的比例式;
(4)试剂瓶标签上氯化钙溶液的溶质质量分数为.
【答案】
分析:(1)根据实验现象的特殊性对于实验数据的采集的作用考虑;
(2)碳酸钙与稀盐酸反应,生成氯化钙、水和二氧化碳,据此写出化学方程式即可;
(3)根据碳酸钙与稀盐酸反应的化学方程式和生成气体的质量,即可列出求解生成氯化钙质量(X)的比例式;
(4)根据(3)的比例式,求出生成氯化钙质量,然后根据“溶质质量分数=
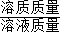
×100%”计算即可.
解答:解:(1)因为碳酸钙与稀盐酸反应有气体生成,可以更好的收集数据;
(2)碳酸钙与稀盐酸反应的化学方程式为:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;
(3)设生成氯化钙质量为x,
CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑
111 44
x 15g+105.4g-111g-5g
∴质量
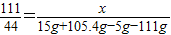
;
解之得:x=11g;
(4)
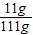
×100%=10%;
故答案为:(1)碳酸钙;
(2)CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;
(3)
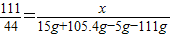
(其它形式也可);(4)10%.
点评:本题主要考查学生利用化学方程式和质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

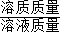 ×100%”计算即可.
×100%”计算即可.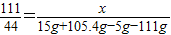 ;
;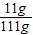 ×100%=10%;
×100%=10%;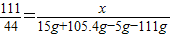 (其它形式也可);(4)10%.
(其它形式也可);(4)10%.

 (2007?哈尔滨)如图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:
(2007?哈尔滨)如图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题: