
3. 铁是一种应用广泛的金属。下列有关铁的叙述正确的是 ( )
A. 铁是地壳中含量最多的金属
B. 工业上用二氧化碳冶炼钢铁
C. 用铁可以回收硝酸银废液中的银
D. 铁丝在氧气中燃烧生成氧化铁 .
科目:初中化学 来源: 题型:
15. 10克黄铜(铜锌合金) 加入装有100克稀硫酸的烧杯中,假定反应物都恰好反应完全,待不再产生气泡时杯中质量减少0.2克,通过计算求:
(1) 黄铜中铜的质量分数为 。
(2) 100克稀硫酸中溶质硫酸质量为 ,溶剂水质量为 。
(3) 反应后所得溶液中溶质质量为 ,溶剂质量为 ,溶液质量为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
9. 某化学兴趣小组对金属的性质做了如下探究,请你填空。
(1) 用下图所示实验探究铁生锈的条件(每支试管中均放有完全相同的洁净铁钉) 。

① 甲同学认为,试管A发生的现象就能够说明铁的镑蚀是铁与空气中的氧气、水蒸气共同作用的结果。乙同学不同意他的观点,认为必须观察试管 (选填试管编号) 发生的现象,并经过科学严谨的推理,才能得出上述结论。
② 试管D和E实验的目的是进一步探究铁在 的环境中是否更容易锈蚀。
③ 为防止金属诱蚀,除了采用覆盖保护膜等措施以外,还可以制成合金。这是因为合金与纯金属相比,其组成和内部组织结构发生变化,从而引起 的变化。
(2) 将一定质量的铁粉放入硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是 ,且反应后溶液质量比反应前 (填“增大”
“减小”或“不变”) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
5.(1) 铝、铁、铜三种金属被发现和使用的先后顺序为铜、铁、铝。金属大规模被使用的先后顺序跟 (选填字母,下同) 关系最大。
A. 地壳中金属元素的含量 B. 金属的导电性 C. 金属的活动性
目前世界上已有50%以上的废钢铁得到回收利用,其目的是 。
A. 节约金属资源 B. 合理开采矿物 C. 防止钢铁生锈
(2) 某同学要验证银、铁、锌的活动性顺序,他已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是 、 。
查看答案和解析>>
科目:初中化学 来源:2015年初中毕业升学考试(山东莱芜卷)化学(解析版) 题型:探究题
将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)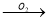 钠的氧化物
钠的氧化物 氢氧化钠溶液
氢氧化钠溶液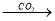 白色固体
白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:
【实验探究一】:
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | 猜想1正确 |
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
实验操作 | 实验现象 | 实验结论 |
1.取少量白色固体加入足量 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入 |
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 。
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为 。
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 碱性氧化物(填“是”或“不是”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
8. 下列现象和事实,可用金属活动性作出合理解释的是 ()
① 金属镁在空气中比铝更易点燃,说明镁比铝活动性强;
② 金属铝比金属锌更耐腐蚀,说明锌比铝活动性强;
③ 硫酸铜、石灰水配制农药波尔多液,不宜用铁制容器;
④ 金属锌与稀硫酸反应速率适中,更适于实验室制取氢气。
A.①② B. ③④ C. ①③④ D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
7.我国具有丰富的钛资源,钛和钛合金是21世纪的重要金属材料,它们具有优良的性能,如熔点高、密度小、可塑性好、机械性能好、抗腐蚀能力强,钛合金与人体有很好的“相容性”。根据它们的主要性能,下列用途中不符合实际的是 ( )
A.用于核潜艇设备的制造 B. 用于制造航天设备
C. 用作电路中的保险丝 D. 可用来制造人造骨
查看答案和解析>>
科目:初中化学 来源: 题型:
4. 下表是NaCl、KN03在不同温度时的溶解度。据此数据,判断下列说法错误的是 ( )
温度/°c | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36. 6 | 37.0 | 37.3 |
KN〇3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
A. KN03和NaCl的溶解度曲线在20〜30°C温度范围内会相交 B. 在60°C时,KN03的饱和溶液l05g加入95g水后,溶液中溶质的质量分数为27. 5% C. 在20°C时,NaCl和KN03固体各35g分别加入两只各盛有l00g水的烧杯中,均不能形成饱和溶液 D. 从含有少量NaCl的KN03饱和溶液中,欲得到较多的KN03晶体可采用冷却热饱和溶液的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com