
| A. | 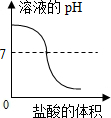 | B. | 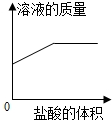 | C. | 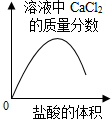 | D. | 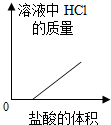 |
分析 A、向一定量的氢氧化钙溶液中逐滴加入稀盐酸,溶液的酸性增强,碱性减弱,恰好反应时,pH=7,酸过量时,pH<7;
B、氢氧化钙与盐酸反应生成氯化钙和水,溶液质量不断增加;
C、氢氧化钙与盐酸反应生成氯化钙和水,氯化钙的质量分数不断增加,氢氧化钙与盐酸恰好反应时氯化钙的质量不变,但随着盐酸不断加入,溶液质量不断增加,氯化钙的质量分数减小;
D、开始加入盐酸会与氢氧化钙反应,当盐酸过量时,溶液中盐酸的质量不断增加
解答 解:A、向一定量的氢氧化钙溶液中逐滴加入稀盐酸,溶液的酸性增强,碱性减弱,恰好反应时,pH=7,酸过量时,pH<7,正确;
B、氢氧化钙与盐酸反应生成氯化钙和水,随着盐酸不断加入,溶液质量不断增加,错误;
C、氢氧化钙与盐酸反应生成氯化钙和水,氯化钙的质量分数不断增加,氢氧化钙与盐酸恰好反应时氯化钙的质量不变,但随着盐酸不断加入,溶液质量不断增加,氯化钙的质量分数减小,正确;
D、开始加入盐酸会与氢氧化钙反应,当盐酸过量时,溶液中盐酸的质量不断增加,正确;
故选B
点评 此题涉及知识面广,与图象结合理解题意,增加思维空间,题的难度较大,因而能考查学生的知识面掌握程度.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
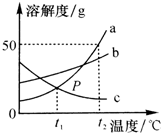 如图是a、b、c三种物质的溶解度曲线,回答下列问题:
如图是a、b、c三种物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
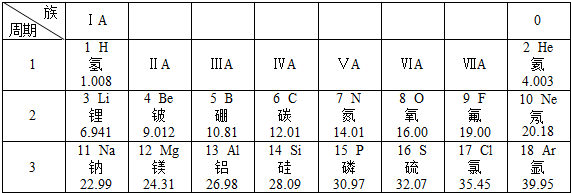
 ,该原子在化学反应中易失去(填“得到”或“失去”)电子.说明元素的化学性质与原子的最外层电子数关系密切,由6、8、11号元素组成的物质的化学式是Na2CO3.
,该原子在化学反应中易失去(填“得到”或“失去”)电子.说明元素的化学性质与原子的最外层电子数关系密切,由6、8、11号元素组成的物质的化学式是Na2CO3.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 10 | 10 | 10 |
| 生成氢气质量/g | 0.04 | 0.04 | 0.02 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com