
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
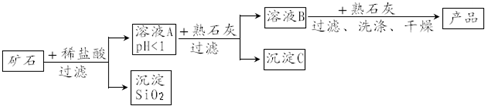
分析 (1)氧化镁和稀盐酸反应生成氯化镁和水,氧化铁和稀盐酸反应生成氯化铁和水,氧化铜和稀盐酸反应生成氯化铜和水;
(2)根据表中提供的信息可以判断相关方密度问题;
(3)稀盐酸和氢氧化钙反应生成氯化钙和水;
(4)氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙;
(5)氢氧化镁受热分解生成氧化镁和水.
解答 解:(1)溶液A中含有的阳离子有镁离子、铁离子、铜离子和氢离子;
氧化镁和稀盐酸反应生成氯化镁和水,氧化铁和稀盐酸反应生成氯化铁和水,氧化铜和稀盐酸反应生成氯化铜和水,反应的化学方程式为:MgO+2HCl=MgCl2+H2O,Fe2O3+6HCl═2FeCl3+3H2O,CuO+2HCl=CuCl2+H2O.
故填:4;MgO+2HCl=MgCl2+H2O,或Fe2O3+6HCl═2FeCl3+3H2O,或CuO+2HCl=CuCl2+H2O.
(2)由表中数据可知,溶液B的pH控制在6.7-8.6时,铁离子、铜离子分别以氢氧化铁、氢氧化铜沉淀析出,而镁离子仍然在溶液中.
故填:6.7-8.6.
(3)溶液B中一定含有的溶质有氯化镁、氢氧化钙和稀盐酸反应生成的氯化钙,可能含有氢氧化钙.
故填:氯化镁、氯化钙.
(4)氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
故填:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
(5)氢氧化镁受热分解生成氧化镁和水,反应的化学方程式为:Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
故填:Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 气体的溶解度随压强增大而增大,所以CO2、SO2的溶解度随压强的增大而增大 | |
| B. | 酸电离出的阳离子是H+,NaHSO4能电离出H+,所以NaHSO4是酸 | |
| C. | 碱性氧化物和水反应生成碱,所以氧化铁与水反应可生成氢氧化铁 | |
| D. | 酸碱指示剂可用于检测溶液酸碱性,所以可用无色酚酞溶液区分盐酸、烧碱溶液和水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
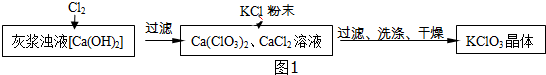
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图所示,在空气中氧气含量的测定的实验,请据图回答下列问题.
如图所示,在空气中氧气含量的测定的实验,请据图回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含钾的化合物 | B. | 含钠的化合物 | C. | 含钙的化合物 | D. | 含铁的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com