
·ÖĪö £Ø1£©Ź×ĻČøł¾Ż·“Ó¦ŌĄķÕŅ³ö·“Ó¦Īļ”¢Éś³ÉĪļ”¢·“Ó¦Ģõ¼ž£¬øł¾Ż»Æѧ·½³ĢŹ½µÄŹéŠ“·½·Ø”¢²½Öč½ųŠŠŹéŠ“¼“æÉ£»
£Ø2£©øł¾Ż½šŹō²ÄĮĻµÄŠŌÖŹĄ“·ÖĪö£»
£Ø3£©ĪøĖįµÄÖ÷ŅŖ³É·ÖŹĒŃĪĖį£¬ÄÜÓėĢś·“Ó¦£»Ģś·ŪÄÜÓėæÕĘųÖŠµÄŃõŗĶĖ®·“Ó¦£¬Ź¹Ģś·Ū±äÖŹ£®
½ā“š ½ā£ŗ£Ø1£©³ąĢśæóµÄÖ÷ŅŖ³É·ÖFe2O3Óė»¹Ō¼ĮŅ»Ńõ»ÆĢ¼·“Ӧɜ³ÉĢś”¢¶žŃõ»ÆĢ¼£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗFe2O3+3CO$\frac{\underline{\;øßĪĀ\;}}{\;}$2Fe+3CO2£®¹ŹĢī£ŗFe2O3+3CO$\frac{\underline{\;øßĪĀ\;}}{\;}$2Fe+3CO2£»
£Ø2£©½«²»ŠāøÖ¼Ó¹¤³ÉČįČķµÄ½šŹōĖæŹĒĄūÓĆĮĖ½šŹōµÄŃÓÕ¹ŠŌ£¬¹Ū²ģŃ”Ļī£¬¹ŹŃ”B£»
£ØĪøĖįµÄÖ÷ŅŖ³É·ÖŃĪĖįÓėĢś·“Ӧɜ³ÉĒāĘų£¬»Æѧ·“Ó¦Ź½ŹĒ£ŗ2HCl+Fe=H2”ü+FeCl2£»ĢśÄÜÓėæÕĘųÖŠµÄŃõŗĶĖ®·“Ó¦Ź¹Ģś±äÖŹ£®¹Ź“š°øĪŖ£ŗFe+2HCl=FeCl2+H2”ü£» ·ĄÖ¹ĢśŌŚ³±ŹŖµÄæÕĘųÖŠ±äÖŹ£¬ŠčŅŖøō¾ųŃõĘų£®
µćĘĄ ±¾Ģāæ¼²éĮĖĢśµÄŅ±Į¶”¢ĢśµÄŗĻ½šµÄĪļĄķŠŌÖŹŗĶ»ÆѧŠŌÖŹ£¬æÉŅŌŅĄ¾ŻŅŃÓŠµÄÖŖŹ¶¼°½šŹō»ī¶ÆŠŌĖ³ŠņµÄŅāŅåĶź³É“ĖĢā£®


 Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø
Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø ±¦±“¼Ę»®ĘŚÄ©³å“Ģ¶į100·ÖĻµĮŠ“š°ø
±¦±“¼Ę»®ĘŚÄ©³å“Ģ¶į100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | MµÄ½šŹō»ī¶ÆŠŌ±ČAgĒæ | B£® | ½šŹōMæÉÄÜŹĒĶ | ||
| C£® | ½šŹōMæÉÄÜŹĒĀĮ | D£® | øĆ·“Ó¦Ē°ŗóMµÄ»ÆŗĻ¼Ū·¢ÉśĮĖøıä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
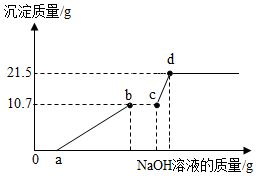 Ļņ 100g ÓÉ FeCl3”¢CuCl2 ŗĶ HCl ×é³ÉµÄ»ģŗĻČÜŅŗÖŠ£¬ĀżĀżµĪ¼Ó NaOH ČÜŅŗ£¬±ßµĪ±ßÕńµ“£¬Ęä·“Ó¦¹ż³ĢČēĶ¼ĖłŹ¾£®ŅŃÖŖ Fe3+ŗĶ Cu2+·Ö±šæŖŹ¼³ĮµķŗĶĶźČ«³ĮµķŹ±ČÜŅŗµÄ pH ČēĻĀ±ķ£®
Ļņ 100g ÓÉ FeCl3”¢CuCl2 ŗĶ HCl ×é³ÉµÄ»ģŗĻČÜŅŗÖŠ£¬ĀżĀżµĪ¼Ó NaOH ČÜŅŗ£¬±ßµĪ±ßÕńµ“£¬Ęä·“Ó¦¹ż³ĢČēĶ¼ĖłŹ¾£®ŅŃÖŖ Fe3+ŗĶ Cu2+·Ö±šæŖŹ¼³ĮµķŗĶĶźČ«³ĮµķŹ±ČÜŅŗµÄ pH ČēĻĀ±ķ£®| Ąė×Ó·ūŗÅ | æŖŹ¼³ĮµķŹ±ČÜŅŗµÄpH | ĶźČ«³ĮµķŹ±ČÜŅŗµÄpH |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| A£® | o”«a ¶Ī”¢b”«c ¶Ī·¢Éś·“Ó¦µÄŹµÖŹ¶¼ŹĒ H++OH-ØTH2O | |
| B£® | a”«b ¶Ī±ķŹ¾ Cu2+Óė OH-·“Ӧɜ³É Cu£ØOH£©2 ³Įµķ | |
| C£® | c µćŹ±ČÜŅŗÖŠµÄČÜÖŹŹĒ CuCl2ŗĶ NaCl£¬pH=7 | |
| D£® | ŌČÜŅŗÖŠFe 3+Óė Cu2+µÄÖŹĮæ±ČĪŖ 10.7£ŗ10.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| Īļ””””ÖŹ | »ÆѧŠŌÖŹ£ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£© | ÓėŠŌÖŹ¶ŌÓ¦µÄÓĆĶ¾ |
| ¢ŁŃõĘų | 2Cu+O2 $\frac{\underline{\;\;”÷\;\;}}{\;}$2CuO | |
| ¢ŚøßĆĢĖį¼Ų | ŹµŃéŹŅÖĘČ”O2 | |
| ¢ŪĒāĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 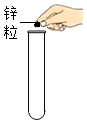 ¾ĄÕż£ŗÓĆÄ÷×Ó¼ŠČ”æéד¹ĢĢå | |
| B£® |  ¾ĄÕż£ŗ¼ÆĘųĘæµ×²æĘĢŅ»²ćĻøɳ | |
| C£® |  ¾ĄÕż£ŗŹŌ¹ÜæŚĀŌĻņĻĀĒ抱 | |
| D£® |  ¾ĄÕż£ŗŹŌ¹Üµ×²æĄėæŖץĆę£¬ÓŅŹÖĪÕ×”Ļš½ŗČū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Įņ·Ū | B£® | ĢśĖæ | C£® | ľĢæ | D£® | ŗģĮ× |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com