
【题目】同学们在学习溶液时,老师用固体M做了如下实验,图一中甲、乙、丙、丁是充分搅拌后静置后的现象,请回答相关问题(忽略水的挥发):

(1)上述烧杯中,溶液质量最大的是_____(填序号);
(2)根据上述实验,可以判断物质M的溶解度曲线是图二对应的_____(填序号);

(3)据图二分析,要使30℃A、B、C三种物质的饱和溶液降温到10℃,所得溶液中溶质的质量分数由大到小的顺序为_____。
【答案】丁 A B>A>C
【解析】
(1)通过分析烧杯中固体溶解的现象,甲烧杯中的溶质是5g,乙烧杯中的溶质小于10g,丙烧杯中的溶质是10g,丁烧杯中的溶质是15g,所以溶液质量最大的是丁;
(2)30℃时,丙烧杯中50g水溶解固体15g后,没有固体剩余,所以M物质的溶解度在30℃时,大于或等于30g,所以判断物质M的溶解度曲线是图二对应的A;
(3)10℃时,B物质的溶解度最大,A物质的溶解度次之,C物质的溶解度最小,降低温度,A、B物质的溶解度减小,C物质的溶解度增大,应该按照30℃时的溶解度计算,所以要使30℃A、B、C三种物质的饱和溶液降温到10℃,所得溶液中溶质的质量分数由大到小的顺序为:B>A>C。
故答案为:(1)丁;(2)A;(3)B>A>C。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:
【题目】菱铁矿(主要成分是FeCO3)是炼铁的原料。现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。
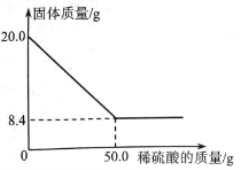
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O
②菱铁矿中杂质不参加反应,且难溶于水。
请计算:
(1)20.0g菱铁矿中FeCO3的质量为 g。
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0。1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乳酸亚铁片可用于治疗缺铁性贫血.下图为乳酸亚铁片说明书上的部分文字.

请仔细阅读后回答以下问题:
(1)乳酸亚铁的相对分子质量为_____,碳、铁两种元素的质量比为_____。
(2)144g乳酸亚铁中铁元素的质量为_____g。
(3)某人每天分二次服药,一次最多服用_____片,服药时不能喝茶的原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)碳及碳的化合物间的转化关系可表示为:![]() ,由此可写出各步反应的化学方程式。
,由此可写出各步反应的化学方程式。
硫及硫的化合物间的转化关系可表示为:![]() 。
。
(1)模仿碳及碳的化合物间转化反应方程式的书写,写出硫及硫的化合物转化反应中指定反应的化学方程式:反应①:____;反应③:____。
(2)反应②中,V2O5在反应前后的质量均为m,则V2O5在该反应中起____作用。
(3)上述反应中,属于化合反应的有:____(填反应序号)。
(4)实验室因操作不当,将浓硫酸滴在书页上,一会书页出现了黑色,且由糊状至烂洞状。这是因为浓硫酸具有____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式书写正确,且元素化合价没有发生变化的是( )
A. 红磷在空气中燃烧 4P+5O2![]() 2P2O5
2P2O5
B. 加热小苏打粉末 2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C. 铜片放入硝酸银溶液中 Cu+2AgNO3═Cu(NO3)2+2Ag
D. 向氯化镁溶液中滴入硫酸钾溶液 MgCl2+K2SO4═MgSO4↓+2KCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有10g49%稀硫酸的烧杯中加入5.6克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是( )
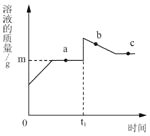
A. 取a点是溶液,加入锌粉,有气体放出
B. b点时,溶液中溶质只有一种
C. c点时,烧杯中固体一定是铜
D. m=12.7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】醋酸CH3COOH是一元有机酸,具有酸的通性.现取溶质质量分数相等的稀硫酸和醋酸溶液等质量,分别放在甲乙两只烧杯中,各加入相等质量的镁粉,生成的氢气的质量比为6:5.则甲乙烧杯中的反应情况可能是( )
A. 甲和乙中金属都过量
B. 甲和乙中酸都过量
C. 甲中酸过量,乙中镁过量
D. 甲中镁过量,乙中酸过量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。

Ⅰ.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用如图所示装置制取NaHCO3,得到的另一种产品NH4Cl,然后再将NaHCO3制成Na2CO3。
(1)写出仪器a的名称_____,装置丙中反应的化学方程式为_____。
(2)装置乙的作用是___________。为防止污染空气,尾气中的__________需要进行吸收处理。
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有___________、___________、___________。
Ⅱ.测定所得产品的组成
(4)检验纯碱样品中是否混有NaHCO3,请选择如图装置设计实验,并完成下表:
选择的装置(填编号) | 实验现象 | 实验结论 |
_____ | _____ | 样品中含NaHCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,蜡烛在一瓶空气中燃烧。利用O2传感器,测定燃烧过程中O2的体积分数,变化如下图所示,下列说法不正确的是
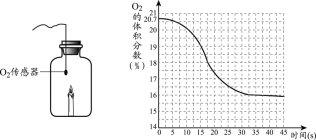
A. 蜡烛燃烧需要氧气
B. 蜡烛熄灭后,密闭容器中还有氧气
C. 蜡烛燃烧前,密闭容器中氧气的体积分数小于21%
D. 蜡烛熄灭后,密闭容器中的二氧化碳体积分数为84%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com